ACS Cent. Sci. 2023 | 什么样的因素造就了优良的蛋白质−蛋白质相互作用稳定剂:双重结合机制的分析与应用
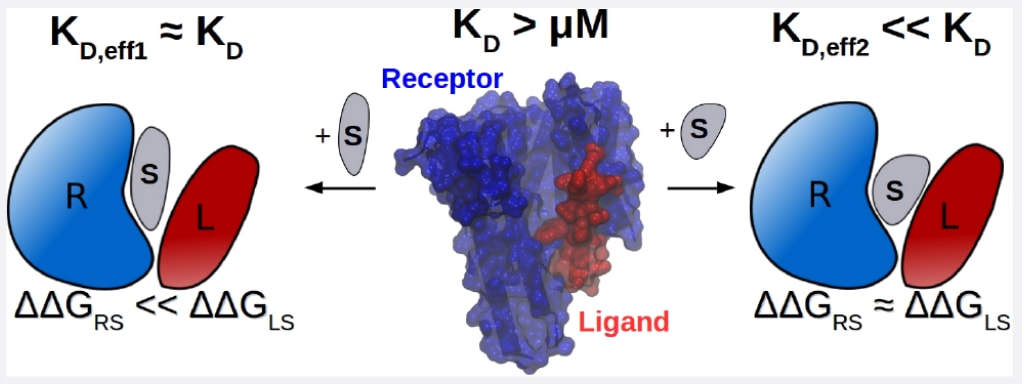
今天介绍的是发表在 ACS Central Science 上的一项研究,题为“什么样的因素造就了优良的蛋白质−蛋白质相互作用稳定剂:双重结合机制的分析与应用”。蛋白质−蛋白质相互作用(PPI)在细胞信号传导、免疫反应以及多种疾病过程中发挥关键作用,因此成为重要的药物靶点。传统研究主要关注通过小分子抑制PPI,但由于蛋白质界面通常较为平坦且缺乏明显结合口袋,许多PPI靶点被认为难以成药。相比之下,通过小分子稳定蛋白质复合物、增强蛋白质之间的相互作用逐渐成为一种新的药物设计思路。该研究通过分子动力学模拟、结合自由能计算以及口袋识别方法,对多种已知PPI稳定剂进行系统分析,并提出“双重结合机制”作为高效稳定剂的重要特征,即稳定剂需要同时与两个蛋白质伙伴产生相近强度的相互作用。相关结果为PPI稳定剂的发现与设计提供了新的理论基础和计算策略。

获取详情及资源:
0 摘要
蛋白质−蛋白质相互作用(protein−protein interactions,PPIs)在免疫反应和多种疾病等生物学过程中发挥关键作用。利用类药物小分子抑制PPI已成为许多治疗策略的基础。然而,在许多情况下,蛋白质复合物界面通常较为平坦,这使得难以在其中一个结合伙伴的腔体中发现能够特异结合的小分子,从而实现对PPI的抑制。另一方面,在蛋白质−蛋白质界面处常常会形成新的结合口袋,这些结构可以容纳稳定剂分子。与抑制PPI相比,稳定蛋白质复合物在很多情况下同样具有重要价值,但这一策略目前仍然研究较少。
通过分子动力学模拟和口袋识别方法,对18种已知稳定剂及其对应的蛋白质−蛋白质复合物进行了研究。结果表明,在大多数情况下,一种“双重结合机制”是实现有效稳定作用的重要前提,即稳定剂需要与两个蛋白质结合伙伴产生相近强度的相互作用。也有少数稳定剂通过变构机制发挥作用,例如稳定蛋白质结合后的构象,或通过间接方式增强蛋白质−蛋白质相互作用。
对226个蛋白质−蛋白质复合物的分析表明,在超过75%的案例中,界面处存在适合类药物分子结合的腔体结构。基于这些发现,提出了一种计算化合物筛选流程,用于利用新形成的蛋白质界面口袋并优化双重结合机制,并将该方法应用于5个蛋白质−蛋白质复合物的研究中。研究结果表明,基于计算方法发现PPI稳定剂具有广阔潜力,并在多种治疗应用中具有重要前景。
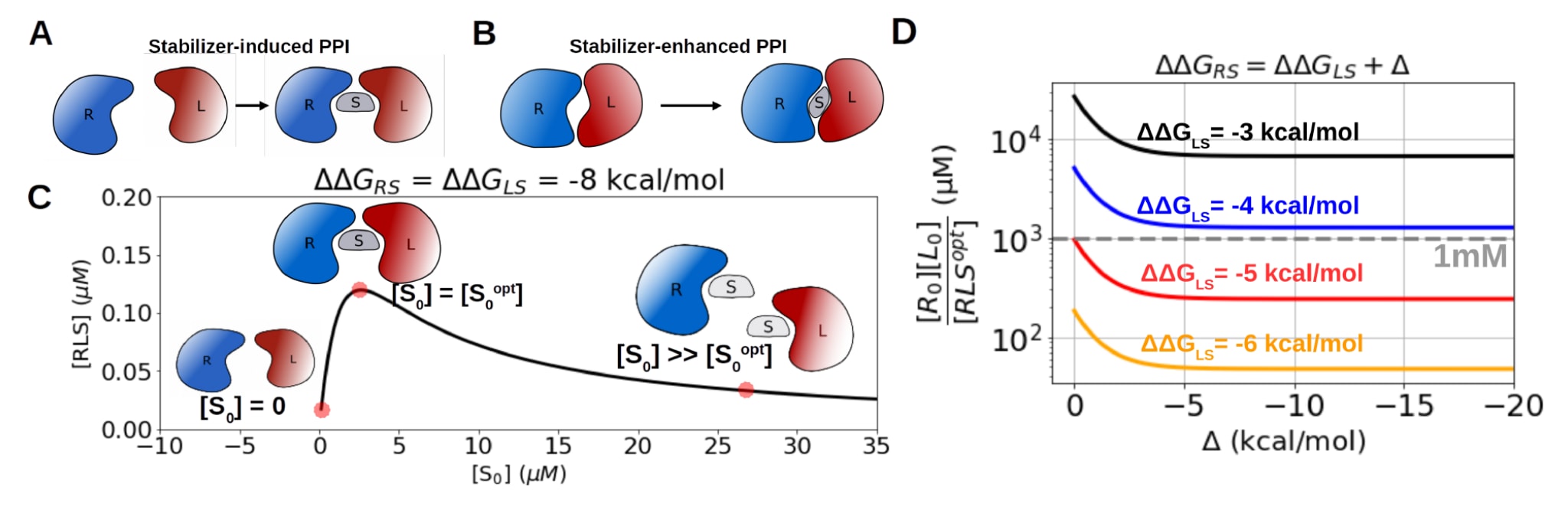
图1|双重结合机制的理论模型。 (A) 稳定剂诱导型PPI示意图。在该情形中,两个原本不相互作用或仅弱相互作用的蛋白质R和L在稳定剂S存在时形成稳定复合物。(B) 稳定剂增强型PPI示意图。在该情形中,本身已经形成的RL复合物在稳定剂S存在时相互作用得到增强。(C) 根据式(1)建立的理论模型示意图。设
1 引言
蛋白质复合物的形成在绝大多数生物学过程中发挥基础性作用,例如细胞命运调控、免疫反应以及信号转导等,同时也与多种人类疾病密切相关,因此为现代药物设计提供了重要的治疗潜力。针对蛋白质−蛋白质相互作用(protein−protein interaction,PPIs)的调控策略通常以抑制为主,但近年来也逐渐关注通过稳定相互作用来实现调控。PPI可以通过变构效应实现抑制,即小分子不一定在界面处结合,而是通过远端结合影响蛋白质构象;也可以通过直接作用于蛋白质−蛋白质界面,使两个蛋白质伙伴无法形成复合物。然而,PPI抑制剂的设计面临一个普遍困难,即蛋白质界面通常较为平坦、埋藏面积较大(通常大于1500 Ų),并且常常具有较强的疏水性,这些特征使其难以被小分子药物有效靶向,因此常被认为是“不可成药”的靶点。
相比之下,较大的肽类抑制剂被认为是一种具有前景的策略,其毒性较低,并且已有多种肽类药物获得临床批准。尤其是具有预定义构象并具备良好细胞通透性的环状肽,在PPI抑制剂设计中受到了越来越多的关注。此外,通过计算方法识别蛋白质界面中的“热点”(hot-spots)并与环状肽进行匹配,也被提出作为一种快速的理性设计策略。
对于许多疾病而言,促进或稳定蛋白质−蛋白质相互作用有时比抑制更为有益。这类稳定作用可以通过小分子有机化合物实现,其机制可以分为两类:一类是变构机制(即不在界面处结合),另一类是直接在蛋白质界面处结合。前一种机制指稳定剂结合到其中一个蛋白质上并产生变构调控,从而提高其与另一结合伙伴的亲和力;后一种机制则是稳定剂直接结合在PPI界面上,并利用界面处可能存在的可成药腔体与小分子相互作用。与PPI抑制剂相比,稳定PPI具有多方面优势,因此在近年来逐渐成为一个新兴研究领域。此前的综述工作对已知的蛋白质−蛋白质−稳定剂复合物进行了系统整理,并根据所稳定的PPI类型以及稳定剂来源对其进行了分类讨论。
目前针对稳定剂设计的药物研发工作仍然相对有限。例如,基于片段的药物发现方法已被用于设计14-3-3适配蛋白与p65来源蛋白之间相互作用的稳定剂,以及针对肿瘤抑制蛋白p53、致癌转录因子TAZ和雌激素受体来源肽的稳定剂。还有研究通过基于结构的虚拟筛选,从Molport数据库中近600万个化合物中筛选候选分子,并对其中13个进行体外实验验证,最终确认其中2个为有效稳定剂。另一项研究结合分子动力学(molecular dynamics,MD)模拟与分子对接技术,对22个14-3-3蛋白−肽−稳定剂复合物进行了分析,并指出20−50 ns的模拟时间结合分子力学泊松−玻尔兹曼表面积(MM/PBSA)与广义Born表面积(MM/GBSA)方法可以有效区分稳定剂与诱饵分子。
随着蛋白质结构预测、蛋白质−蛋白质对接以及蛋白质复合物结构预测技术的快速发展,仅基于蛋白质序列信息预测潜在PPI稳定剂也逐渐成为一种成本较低且具有前景的研究路线。为了实现这一目标,深入理解已有稳定剂的作用机制具有基础性意义。
该研究首先讨论PPI稳定的理论基础,并强调“双重结合机制”(dual-binding mechanism)的重要性。随后利用分子动力学模拟并结合蛋白质伙伴与稳定剂之间的相互作用自由能计算,对已有的蛋白质−蛋白质复合物及其稳定剂进行分析。研究中将无法在没有稳定剂情况下形成复合物的情况称为稳定剂诱导的PPI(stabilizer-induced PPI)(图1A),而将本身即可形成复合物但在稳定剂存在时相互作用增强的情况称为稳定剂增强的PPI(stabilizer-enhanced PPI)(图1B)。
分析结果表明,在大多数情况下,更高效的稳定剂在与两个蛋白质伙伴之间分配相互作用时较为均衡,而这种分布与稳定剂与蛋白质复合物之间的总相互作用自由能大小无关。这一现象与基于平衡结合状态建立的数学模型预测一致;相比之下,稳定效果较弱的稳定剂往往更倾向于与其中一个蛋白质形成更强的相互作用。不过,也有少数化合物通过变构机制间接提高蛋白质−蛋白质亲和力从而实现稳定作用(18个案例中的4个)。此外,还观察到稳定剂对蛋白质伙伴之间直接相互作用产生的间接正向或负向(去稳定化)影响。
研究还发现,约80%的稳定剂结合口袋可以通过对没有稳定剂的蛋白质复合物晶体结构进行直接计算探测而识别出来。对于那些在静态结构中被隐藏的口袋,通过进行短时间MD模拟并随后进行口袋检测即可揭示。结果还表明,双重结合机制可以作为识别潜在PPI稳定剂的重要依据。
基于上述模型,提出了一种用于发现PPI稳定剂的计算流程,该流程结合了口袋探测、分子对接以及MD模拟。同时对大量已知蛋白质复合物进行了分析,发现约75%的案例在界面处存在适合稳定剂结合的可成药腔体,并将所提出的方法应用于其中5个蛋白质复合物。结果显示,该策略在基于结构的PPI稳定剂药物设计中具有良好的应用前景。
2 结果与讨论
2.1 通过双重结合机制实现PPI稳定化
高效的PPI稳定剂的目标通常是提高RLS三元复合物的形成水平。在受体R与配体L本身不发生相互作用的情况下,例如稳定剂诱导型PPI,该体系类似于Yang和Hlavacek所讨论的双价支架体系(图1A)。设受体、配体以及稳定剂的总浓度分别为
其中
在上述表达式中,
在该浓度下RLS复合物达到最大值
利用关系式
这一结果表明,与稳定剂结合较弱的蛋白质,即
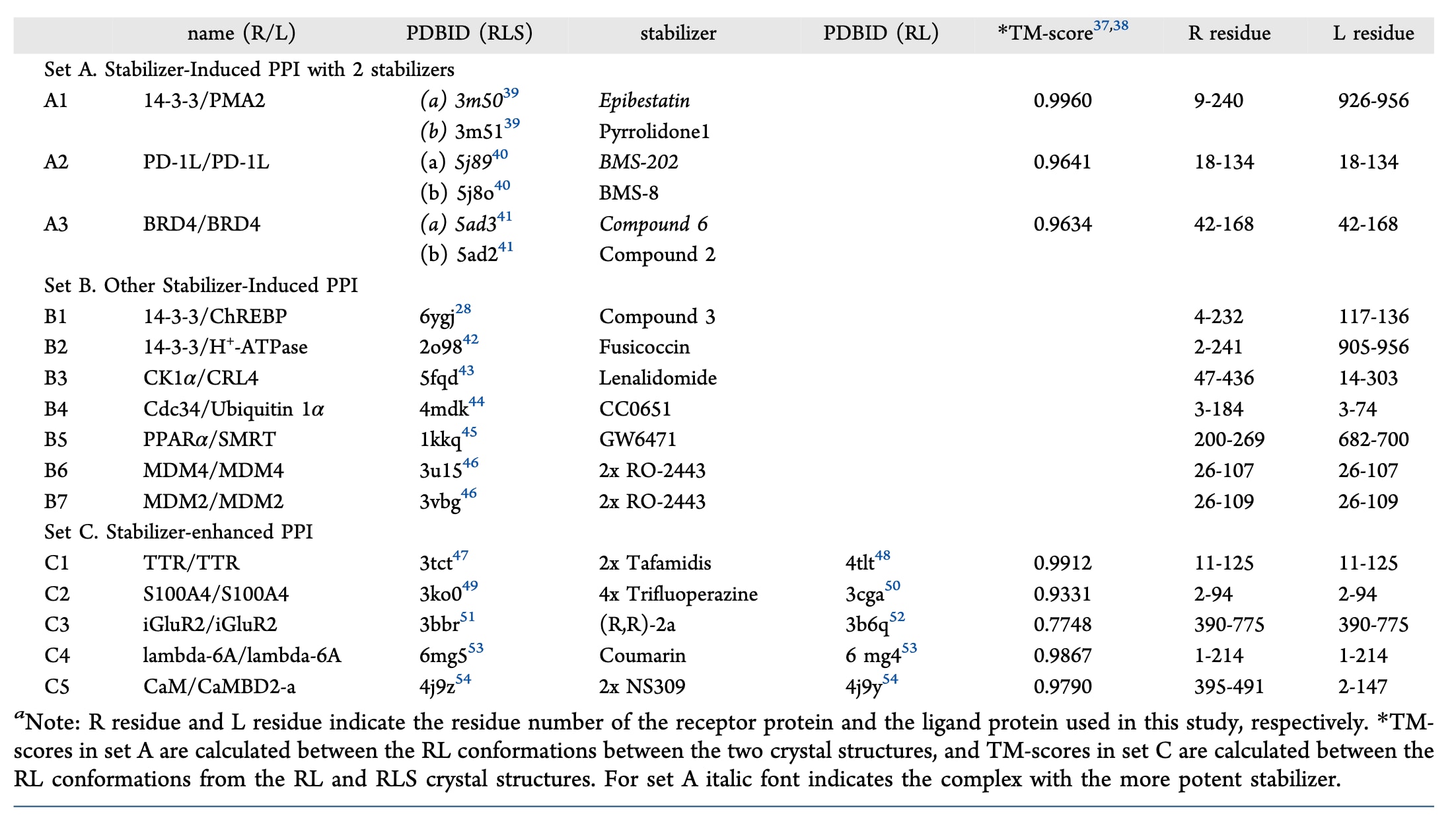
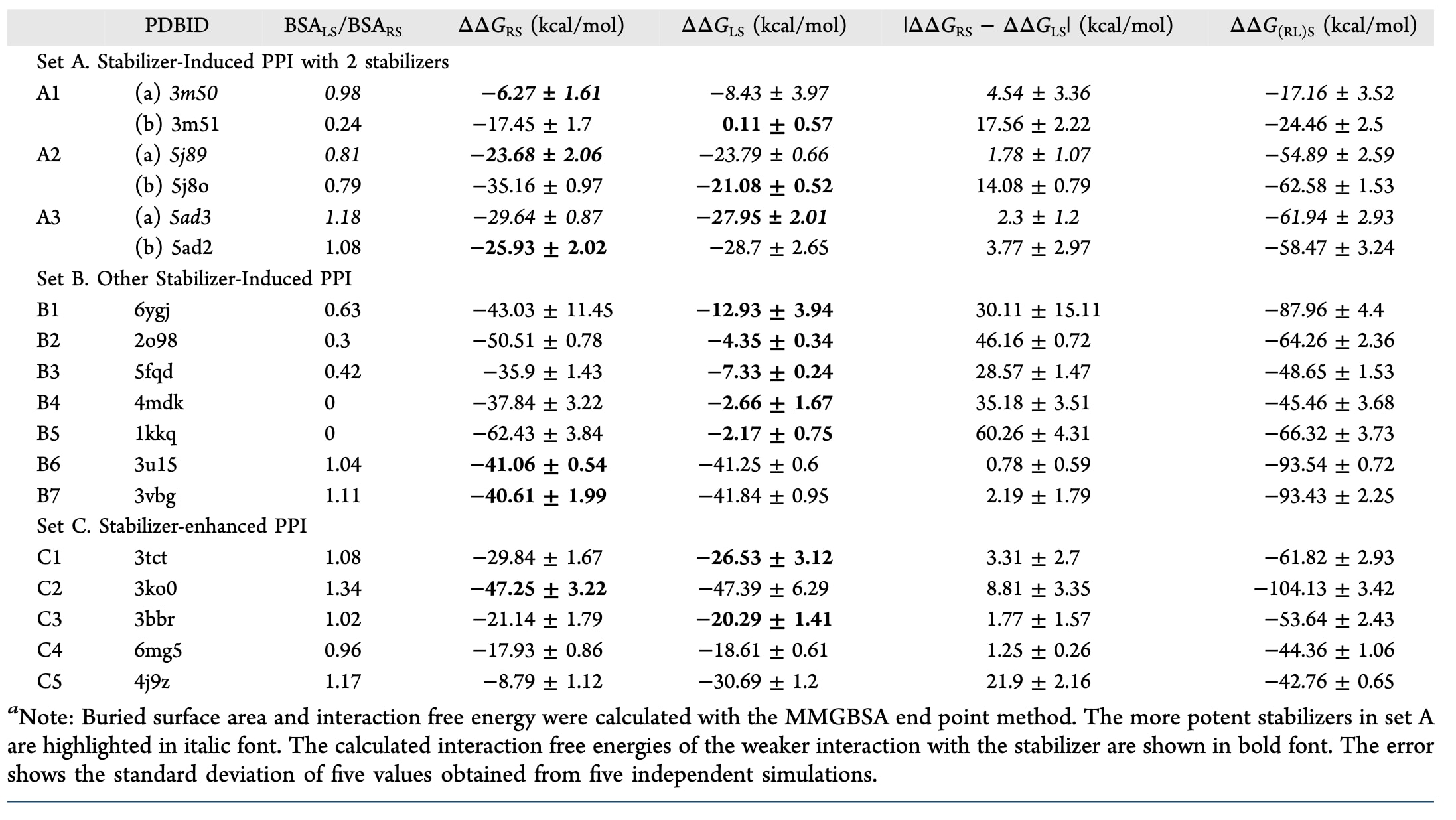
表1|该研究中分析的由小分子稳定的蛋白质−蛋白质复合物。
2.2 已知稳定剂结合的蛋白质复合物分析
研究中利用分子动力学模拟与口袋检测方法,对18种稳定剂与15种不同PPI体系进行了分析。数据集概况见表1,并在图2中进行了可视化展示。一个被稳定的PPI体系通常包含受体蛋白(R)、配体蛋白(L,通常为较小的蛋白质伙伴)以及稳定剂(S),统称为RLS复合物;而没有稳定剂参与的蛋白质复合物则称为RL复合物。
具有三维结构信息的15个PPI体系被划分为三个数据集。数据集A包含3个稳定剂诱导型PPI,其中同一R−L蛋白对受到两种不同稳定剂的稳定作用,并且实验上测定了稳定效果并获得了共晶结构。该数据集用于研究实验测得的稳定效率与RLS复合物的结构、动力学及热力学性质之间的关系。数据集B包含另外7个稳定剂诱导型PPI(每个体系只有一种稳定剂的复合物结构),以及来自数据集C的5个稳定剂增强型PPI(这些体系同时具有无稳定剂情况下的三维结构)。
例如在A1体系中,14-3-3蛋白与PMA2的C端结构域之间的复合物可以由二肽Epibestatin(A1-a,
尽管不同稳定剂在相互作用表面上存在差异,但首先比较稳定剂与两个蛋白质伙伴之间的界面面积仍然具有参考价值。因此,计算了18个RLS复合物中RS与LS界面的埋藏表面积(BSA),以快速估计稳定剂与蛋白质之间的接触情况(图3A)。结果显示,大多数稳定剂与两个蛋白质伙伴之间具有相似的BSA,说明稳定剂与两种蛋白质之间的接触数量大致相当(表2)。然而有趣的是,在A2与A3体系中,稳定效果更强的稳定剂(A2-a和A3-a)反而与R和L形成较小的BSA。此外,还观察到A1-b、B2、B4以及B5中的稳定剂与配体蛋白几乎没有接触,这显然不符合前述双重结合机制的要求。
为了更准确地评估相互作用,进一步进行了分子动力学模拟,并利用MMGBSA终点方法计算稳定剂与受体之间的相互作用自由能
然而,B2、B4和B5中的稳定剂并不符合这一规律,并且这些稳定剂与配体蛋白之间的计算相互作用自由能
为了进一步理解这些稳定剂在没有双重结合的情况下如何诱导RLS复合物形成,去除了配体蛋白并分别在有稳定剂(R+S)和无稳定剂(R only)条件下进行了200 ns的MD模拟。结果发现,在存在稳定剂时,受体界面残基(即在RLS复合物中与配体接触的残基)保持稳定,而在移除稳定剂后这些残基的运动性显著增加,界面均方根偏差(iRMSD)明显升高(图3C−D)。这说明在这些体系中,稳定剂主要结合于一个蛋白质伙伴(受体),并稳定其结合构象,从而通过变构效应促进蛋白质复合物的形成。
随后计算了稳定剂存在时与不存在时受体和配体之间的直接相互作用能
为了理解这一现象,对RL复合物进行了基于残基的能量分解分析,从而识别有利接触(负结合能)和不利接触(正结合能)。分析结果显示,在稳定剂诱导型PPI体系中,不利的RL接触往往由参与稳定剂结合的残基形成。因此,除了双重结合机制之外,稳定剂还可以通过遮蔽这些不利的RL相互作用来提高整体结合稳定性。
这一机制也解释了为什么数据集A中的受体和配体在稳定剂结合后通常形成相似构象,即在形成有利RL接触的同时,在不利接触附近形成可结合小分子的腔体。当稳定剂从这些RLS复合物中移除后,这些不利接触重新暴露,从而导致界面结构发生扭曲。这种效应在A3、B6以及B7体系中在50 ns模拟内即可观察到(图3F及补充图S3、S4)。相比之下,稳定剂增强型PPI体系在没有稳定剂时界面仍然保持稳定(图S5)。这些稳定剂通常涉及大量有利的RL接触,因此更可能对直接的RL相互作用产生干扰(图3G及补充图S6)。
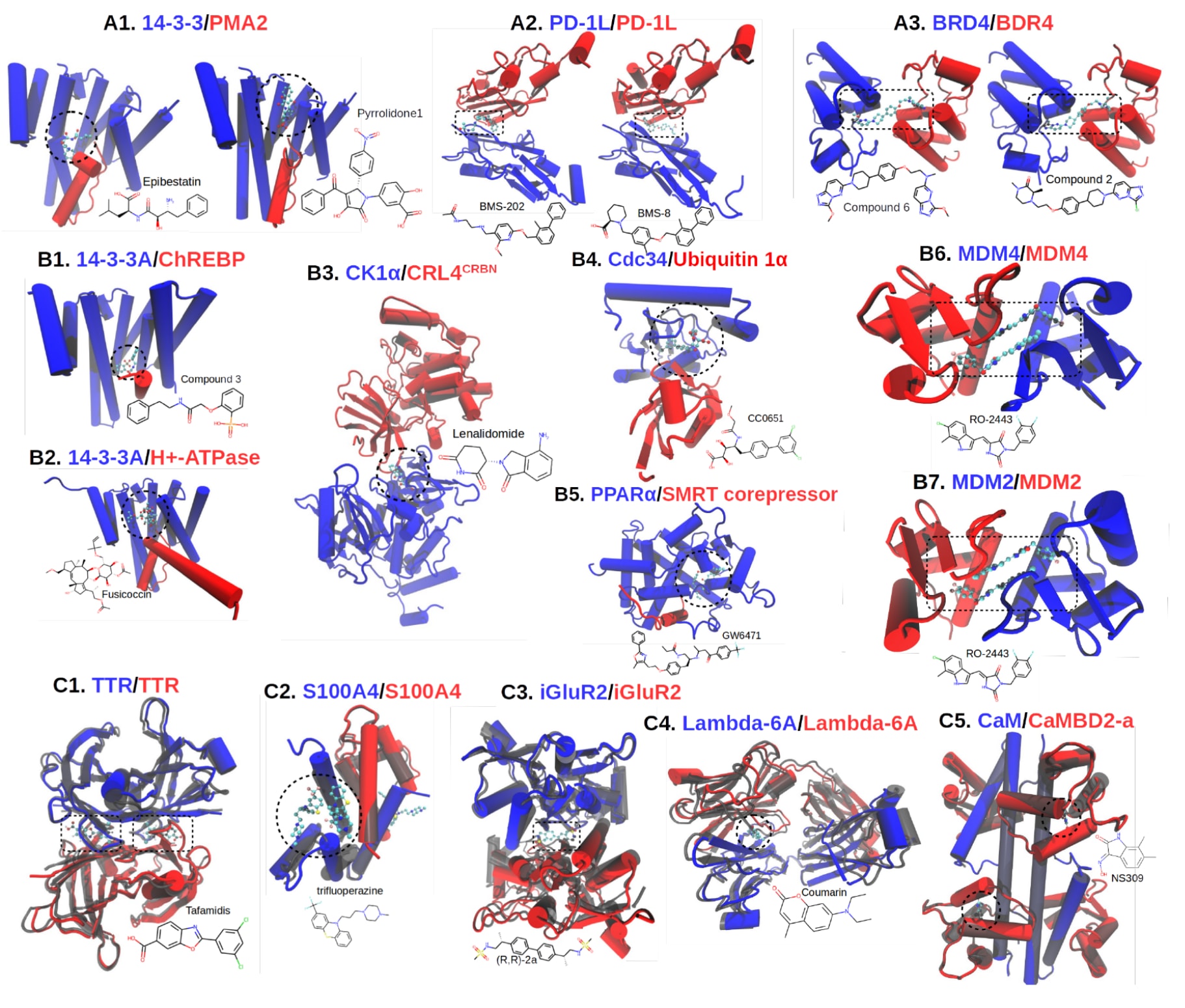
图2|该研究分析的RLS三元复合物的三维结构。 受体蛋白与配体蛋白分别以蓝色和红色表示。对应的PDB编号列于表1。稳定剂的位置以黑色虚线圈出。数据集A(第一行)包含6个RLS复合物,这些体系具有相同的RL蛋白伙伴,并分别与更强稳定剂(左)和较弱稳定剂(右)结合。数据集B(中间各行)包含7个仅具有稳定剂复合物结构、但缺少RL复合物结构的RLS体系。数据集C(最后一行)包含5个同时具有RLS复合物结构以及RL复合物三维结构的体系,其中RL复合物以半透明灰色表示。
2.3 MD模拟揭示隐藏的稳定剂结合口袋
在基于结构的药物设计(structure-based drug design,SBDD)框架下发现潜在的PPI稳定剂时,识别具有利用价值的配体结合口袋是关键步骤。结构比较表明,PPI稳定剂能够结合在RL复合物界面处的口袋中,而不会显著改变复合物的整体构象(表1),这为虚拟筛选提供了可能。研究利用Fpocket4.0对天然RL复合物进行口袋探测,在每个RL复合物中至少识别出10个潜在口袋(图4A)。
尽管双重结合机制已经排除了非界面口袋,但如果对所有可能的界面口袋进行虚拟筛选,计算成本仍然较高,因此需要一种可靠的方法对界面口袋进行排序,从而缩小需要探索的构象空间。为了评估Fpocket提供的评分指标,例如drug score和pocket score,是否能够有效区分稳定剂结合口袋与其他界面口袋,研究计算了每个口袋的配体覆盖比例(具体方法见Methods)。结果表明,除了C4复合物之外,其余所有稳定剂结合口袋都可以在RL复合物结构中完全或部分检测到,并且在pocket score和drug score排名中表现良好。这说明仅基于RL复合物结构就能够可靠地识别潜在的稳定剂结合口袋(图4B)。
进一步利用MDpocket对模拟过程中稳定剂结合口袋的动态变化进行追踪(方法见Methods)。结果显示,所有口袋在模拟中都表现出明显的“呼吸式”运动,即口袋体积在一定范围内不断变化(图4C,时间序列见补充图S7)。特别是在C4复合物中,虽然稳定剂结合口袋在RL晶体结构中是隐藏的,但在模拟过程中其体积会偶尔扩展到足以容纳稳定剂分子的大小,并伴随快速的体积波动(图4C及补充图S7)。
当从RLS复合物中移除稳定剂后,在少数情况下稳定剂结合口袋的体积在模拟过程中变化不大;然而在许多体系中,口袋体积分布明显减小,并且经常采样到小于配体体积的口袋(图4D)。在A3、B6以及B7体系中,移除稳定剂会导致RL界面发生结构扭曲,使得稳定剂结合口袋完全无法被检测到(补充图S3、S4、S8和S9)。需要指出的是,在稳定剂诱导型PPI体系中,由于蛋白质之间的相互作用本身较弱,如果模拟时间延长至更长尺度(例如微秒级),界面结构扭曲甚至RL复合物解离都是可以预期的。
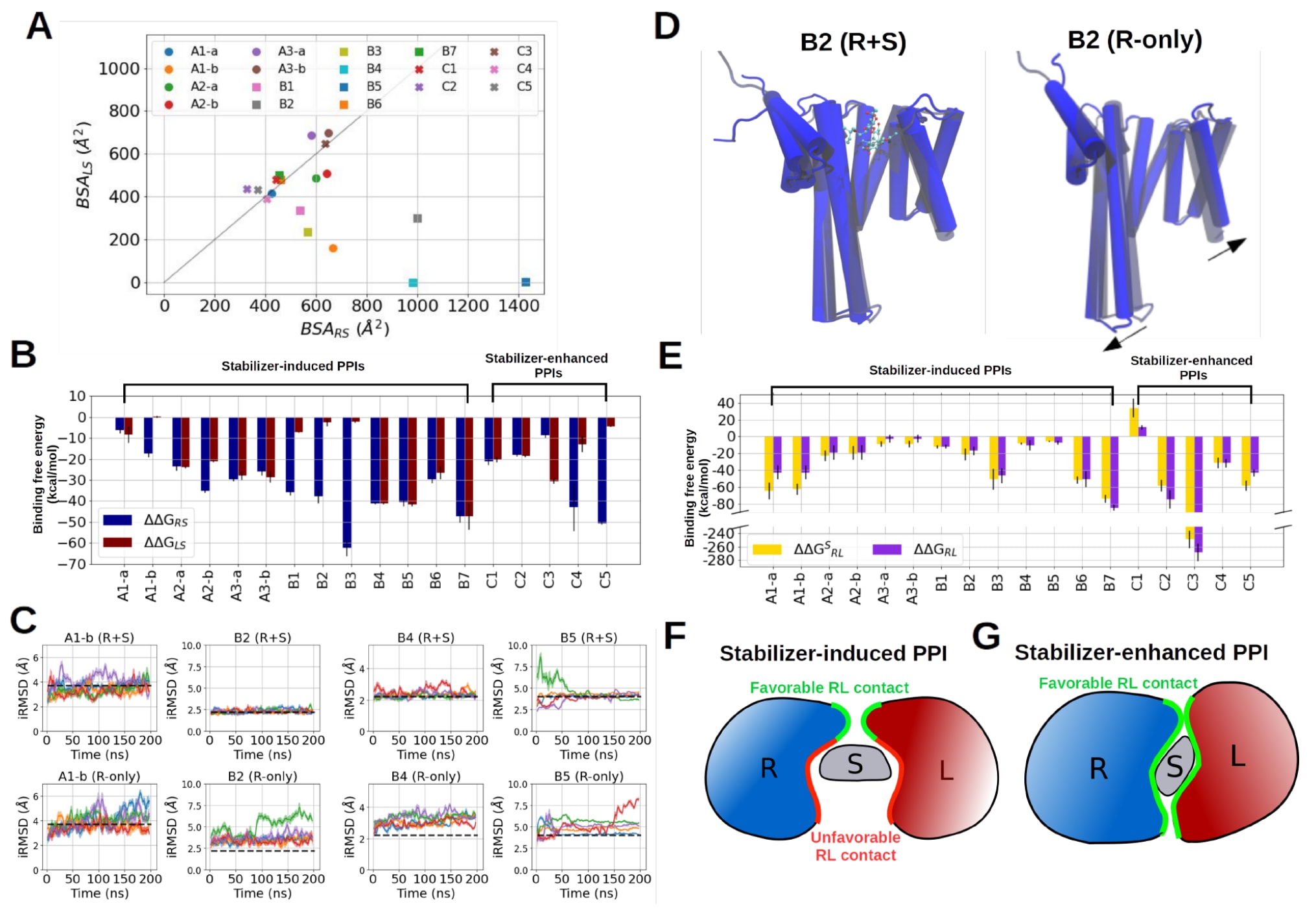
图3|基于MD模拟的结合自由能与界面稳定性分析。 (A) 表1所列RLS晶体结构中,配体与稳定剂之间的埋藏表面积
2.4 双重结合机制在计算识别PPI稳定剂中的应用
对18种PPI稳定剂的系统研究揭示了PPI稳定化的作用机制以及稳定剂结合口袋的动态特性。特别是基于初始理论模型提出并得到实验结果支持的“双重结合机制”表明,稳定剂与相互作用较弱的蛋白质伙伴之间的结合亲和力在RLS三元复合物形成过程中起决定性作用。因此,与传统的基于结构的药物设计(SBDD)流程相比,该机制可能提供更有效的化合物排序策略。传统方法通常仅考虑化合物与目标蛋白之间的总相互作用能,而忽略稳定剂在两个蛋白质伙伴之间相互作用的平衡关系。
为了验证双重结合排序策略的有效性,在14-3-3/ChREBP复合物体系中进行了测试。该体系包含Sijbesma等人通过虚拟筛选预先筛选出的13种候选化合物(见补充图S10A)。通过分子对接、MD模拟以及MM/GBSA计算对这些化合物的双重结合行为进行分析(方法见Methods,补充图S10B)。结果表明,这些化合物在计算上普遍表现出与受体之间的相互作用强于与配体之间的相互作用(图5A)。根据双重结合机制,稳定效果的关键在于化合物与相互作用较弱的配体蛋白之间的结合强度。因此,当以配体结合亲和力而不是受体结合亲和力或总结合能对化合物进行排序时,其结果与实验数据之间的一致性得到明显提高(图5A)。
表2|RL复合物与RLS复合物中平均相互作用能的计算结果。
基于这些观察,提出了一种适用于PPI稳定剂发现的计算流程(图5B)。首先需要获得目标RL蛋白对的三维结构,可以来自实验结构,也可以通过蛋白质复合物建模获得。随后利用Fpocket对PPI界面上的可成药口袋进行探测和排序,并通过MD模拟评估口袋的稳定性或探索隐藏口袋。当确定合适的结合口袋后,可以利用分子对接程序对大型化学数据库进行虚拟筛选(具体流程见Methods)。对接得分较高的化合物随后进行MD模拟,以评估其结合稳定性和相互作用自由能。在这一阶段,需要特别关注化合物与两个蛋白质伙伴之间的相互作用是否具有相似强度,因为根据双重结合机制,这种平衡有助于实现最佳稳定效果。最终,符合这些条件的化合物可以进入实验验证和先导化合物优化阶段。
为了展示该流程的可行性,将该方法应用于protein docking benchmark set 5.0中的一部分数据,该数据集包含226个高质量蛋白质复合物。口袋检测结果表明,在226个复合物中,有223个(98.7%)至少存在一个由界面两侧各5个原子组成的口袋;173个(76.5%)存在由界面两侧各至少10个原子组成的口袋;57个(25.2%)存在由界面两侧各至少20个原子组成的口袋(补充图S11A−B)。进一步从这些体系中提取由两个蛋白质各至少5个原子组成且评分最高的界面口袋,识别出多个潜在口袋,其中一些口袋的pocket score和drug score甚至高于前文分析的已知稳定剂结合口袋(图4B,补充图S11C−D)。
在这些候选口袋中选择了5个具有较高drug score的界面口袋用于虚拟筛选,分别来自PDBID 1AK4、1Y64、2GAF、3H11和4FZA(图5C)。随后从ZINC20数据库中选择100万种化合物,对这些界面口袋进行分子对接(方法见Methods)。结果表明,除drug score最低的口袋(PDBID 3H11,score=0.812)外,其余口袋均能够容纳超过75%的筛选化合物,并获得优于−6 kcal/mol的对接得分,说明基于drug score预筛选的口袋具有良好的成药潜力(图5D)。
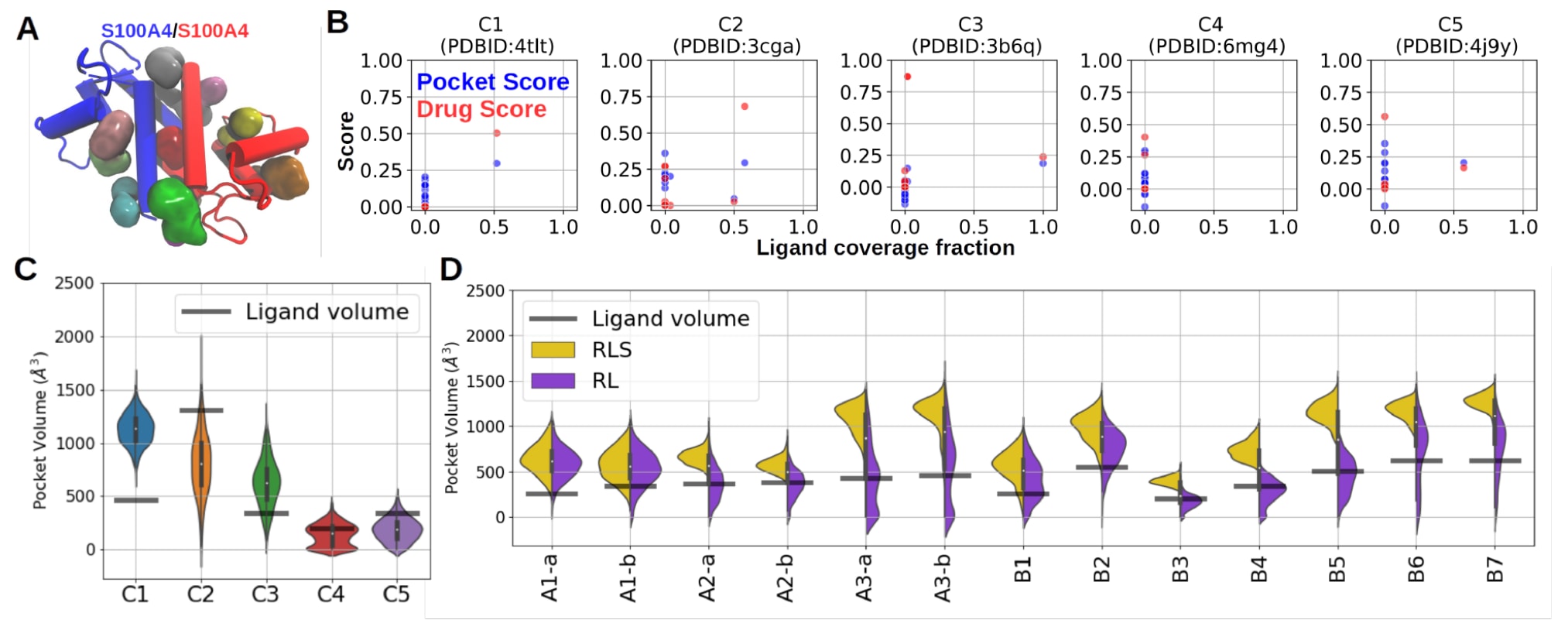
图4|通过MD模拟进行界面口袋的识别与发现。 (A) 以C2 RL复合物(PDBID:3cga)为例,展示Fpocket检测得到的口袋示意图。(B) 配体覆盖比例与Fpocket评分之间的相关关系。(C) 数据集C中稳定剂结合口袋体积在MD模拟中的分布情况。(D) 数据集A和B中稳定剂结合口袋体积在MD模拟中的分布,其中黄色表示稳定剂存在状态(RLS复合物),紫色表示无稳定剂状态(RL复合物)。配体体积通过http://www.scfbio-iitd.res.in/Sanjeevini/Molecular-volume-calculator.php计算,并以半透明线表示。
对于每个蛋白质复合物,对接得分最高的10个化合物及其得分列于补充图S12−S16,并进一步进行MD模拟以计算相互作用自由能(补充表S1−S5)。研究表明,一个理想的PPI稳定剂通常具有两个重要特征:其一是与相互作用较弱的蛋白质伙伴具有较强结合能力,即
其中,在4FZA蛋白质界面筛选得到的前三个化合物(compound 5、compound 8和compound 9,补充表S5)均表现出
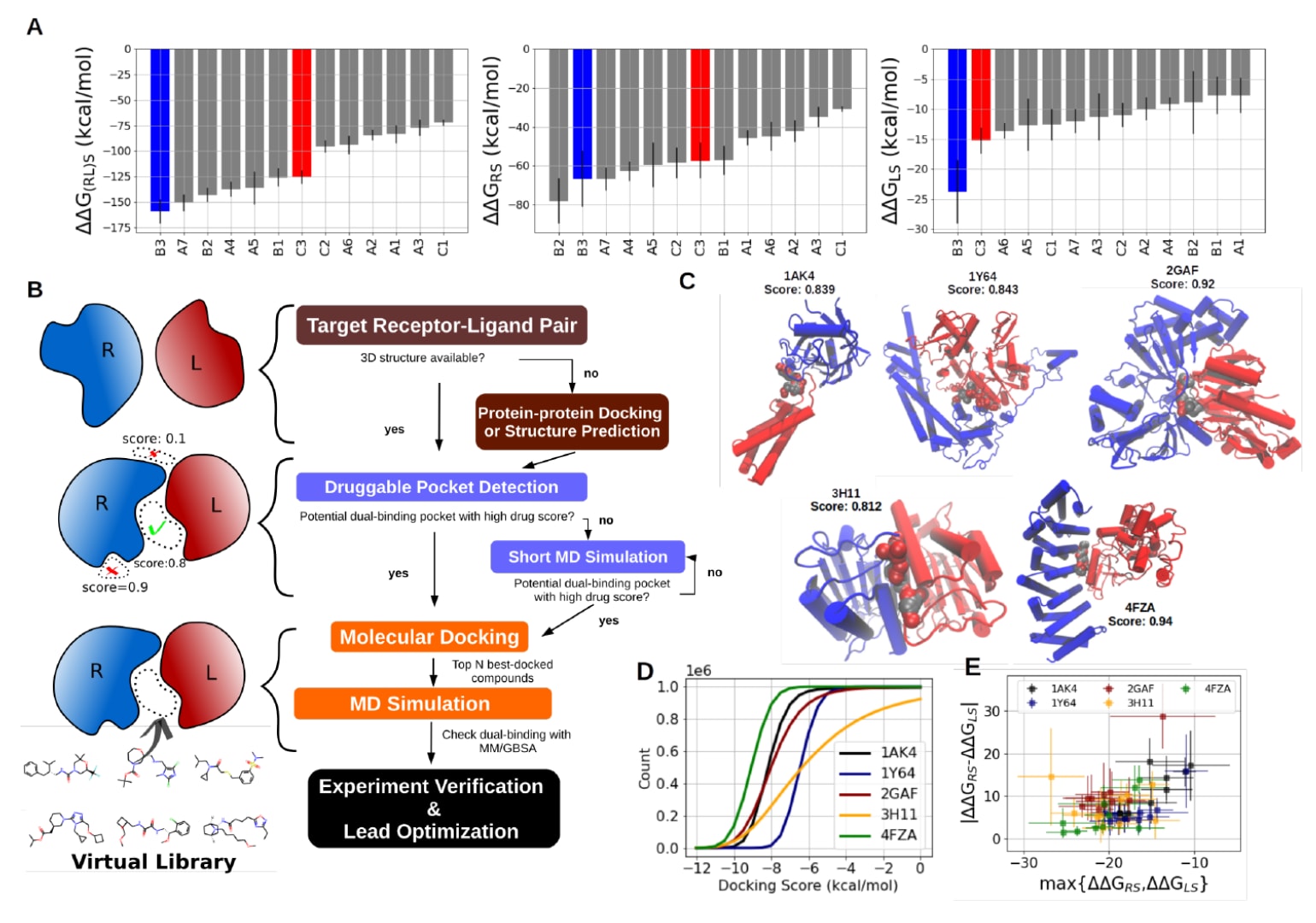
图5|双重结合机制在PPI稳定剂发现中的应用。 (A) 对13个潜在的14-3-3/ChREBP稳定剂进行重新排序,分别基于总结合能(左,
3 讨论
为了促进PPI稳定剂的开发,有必要深入理解这些化合物如何稳定蛋白质复合物。在该研究中,通过分子动力学模拟、相互作用自由能计算以及口袋检测方法,对18种稳定剂在其对应蛋白质复合物中的结合行为进行了系统分析。研究表明,稳定剂可以通过双重结合机制以及对受体(或配体)结合构象的稳定作用来促进PPI复合物的形成。更常见且更有效的机制是双重结合机制,即稳定剂需要与两个蛋白质伙伴产生大致相当的相互作用。在这种机制下,稳定效果主要由与稳定剂结合较弱的蛋白质伙伴所决定。此外,稳定剂还可以通过遮蔽原本不相互作用的RL蛋白对之间的不利接触,同时不影响有利接触,从而促进复合物形成。
研究还发现,一部分不满足双重结合机制的稳定剂仍然能够促进PPI复合物形成,其作用方式是稳定其中一个蛋白质界面,使其保持一种更有利于与另一蛋白结合的构象。这种更加复杂的变构机制理论上可以通过对蛋白质在有无稳定剂条件下进行长时间MD模拟来检测。然而,这类模拟结果可能受到力场误差的影响,同时计算成本较高,因此在需要评估大量候选化合物时并不十分实用。基于这一考虑,在实际的药物设计过程中,更可行的策略是优先寻找符合双重结合机制的潜在稳定剂。
对实验结构中稳定剂结合口袋的分析表明,大多数稳定剂结合口袋可以直接从未结合稳定剂的RL复合物结构中识别出来。对于那些在静态结构中被隐藏的口袋,通过短时间MD模拟即可显现出来。此外,在大量已知蛋白质复合物结构中也可以检测到能够容纳配体并支持双重结合机制稳定作用的界面口袋,并且这种情况在多数体系中都存在。
基于上述分析,研究证明双重结合机制可以作为识别高效稳定剂的重要依据,并提出了一套用于发现PPI稳定剂的计算流程。该流程被应用于5个测试体系,并成功提出了针对5个蛋白质复合物的潜在PPI稳定剂候选分子。通过结合口袋评分方法与双重结合判据,该基于结构的药物设计流程能够有效识别具有成药潜力的界面口袋,并在计算层面评估其稳定化能力。
随着蛋白质结构预测和蛋白质−蛋白质对接技术的不断进步,未来有可能设计出能够诱导特定蛋白质之间形成复合物的小分子。对于已知的相互作用几何构型,该研究提出的方法同样可用于寻找能够诱导PPI形成或增强弱相互作用的化合物。该研究是首个系统性计算研究,全面分析不同类型PPI稳定剂的结合行为。相关结果预计将为未来PPI稳定剂的发现与开发提供重要参考。