BioDesign Research 2025 | 基于七肽插入法的ROP蛋白延伸与结构生物学研究
今天介绍的这项工作来自 BioDesign Research。该研究围绕一种结构高度规则、稳定性突出的四螺旋束蛋白——大肠杆菌ROP蛋白,系统探索了通过七肽重复插入实现蛋白长度精确延展的工程策略。研究以结构和性质已被充分表征的ROP蛋白为基础,在保持其折叠方式、刚性和热稳定性的前提下,将蛋白长度从4.3nm成功延长至6.5nm,实现了50%的线性增长。通过逐步引入色氨酸以增强定量能力、插入七肽重复以延展螺旋束、并在核心重新引入芳香残基以提高序列多样性,作者构建并解析了多个高分辨率晶体结构,验证了设计的可行性与结构一致性。研究结果表明,平行α螺旋束可以通过理性设计在不牺牲稳定性的情况下实现模块化延长,为构建具有精确几何尺寸的蛋白质纳米构件提供了可靠范式,尤其在抗体构象测量与蛋白质计量学等领域具有重要应用潜力。

Karageorgos, I.; Gallagher, D. T. Heptad Insertion Extends the E. Coli ROP Protein by 50 %. BioDesign Research 2026, 8 (1), 100061. https://doi.org/10.1016/j.bidere.2025.100061.
0 摘要
抗体的功能依赖于其构象可变性,但其极高的柔性同时也使结构与性质的测量变得复杂。抗体还能够结合多种配体,这提示如果构建一种长度合适且结构刚性的双价配体,有可能与抗体相互作用,从而在成像、测量或功能调控中降低其构象柔性。理想情况下,这类构件应包含一个相对刚性、长度位于6至10nm之间的配体间隔结构。由α螺旋组成的卷曲螺旋束是蛋白质结构中常见的一类模体,其平行排列的几何特征较为简单,适合进行理性改造,并可应用于计量学相关研究。在该研究中,提出了一种通过七肽重复插入来延展螺旋束的设计思路,并将其应用于大肠杆菌ROP/ROM蛋白。该蛋白是一种分子量约13kDa、耐热的RNA结合单元,自然状态下形成四螺旋二聚体,并已被工程化用于以多种方式自组装成更大的结构。研究首先在蛋白核心中引入一个色氨酸残基,以支持精确定量,野生型蛋白本身不含色氨酸,随后通过插入四个螺旋七肽将蛋白长度延展至其天然长度的150%。文中系统报道了工程化设计过程,以及色氨酸突变体和延长型蛋白的晶体结构,后者在核心中还包含一个新引入的苯丙氨酸残基。野生型ROP蛋白长度为4.3nm,而延展变体的长度达到6.5nm,有望作为高阶蛋白构建中的刚性模块使用。
1 引言
包括抗体在内的生物药物性质测量对于其有效性控制和安全性保障具有重要意义。通过多种实验方法测得,抗体两个抗原结合位点之间的距离通常分布在6至14nm范围内。该结合位点间距对抗体的双价结合功能和信号传导至关重要,但其在溶液中的变化范围及构象集合分布却难以精确测量。现有测量手段的局限性表明,引入一种正交的方法来评估单克隆抗体的柔性,有助于提升相关预测模型的准确性。作为构建基于蛋白质的纳米尺度计量工具的一步尝试,该研究构建并表征了一种延长型的大肠杆菌ROP蛋白。该变体在保持ROP蛋白已知且高度精确的四螺旋束结构的同时,其长度增加了50%,从而进入IgG1抗体两个结合位点间距的预测范围。
大肠杆菌ROP蛋白具有良好的稳定性和简洁的结构排列,使其在蛋白质结构研究早期即发挥了重要作用。同时,该蛋白也被广泛应用于质粒中,用于在大肠杆菌异源表达体系中行使其天然的质粒拷贝数调控功能。ROP作为一种负调控因子,通过增强RNA I与RNA II两种RNA分子之间的相互作用来调节ColE1家族质粒的拷贝数。野生型ROP蛋白为分子量约13kDa的二聚体四螺旋束结构,既被称为引物抑制蛋白,也被称为RNA一调节蛋白。已有研究表明,ROP的多种突变可引发广泛的几何构型和四级结构重排,这些研究为蛋白折叠与稳定性分析以及卷曲螺旋蛋白工程设计规则的建立提供了重要依据。这类研究得益于ROP普遍具有良好的热稳定性,并且在多种工程化变体和晶体形式中均表现出优异的衍射性质。最初解析的野生型ROP结构分辨率为1.7Å,而部分工程化变体的分辨率可达1.1Å。ROP高度规则的结构使得研究者能够系统分析不同结构要素在蛋白性质中的作用,包括环区、螺旋主链、螺旋之间的相互作用以及核心堆积方式,从而揭示蛋白折叠与稳定性背后的能量学因素。研究表明,核心残基突变可以在不改变整体结构的情况下影响折叠行为,而环区突变则可能在保持单条螺旋结构的同时改变整体构型。A31P突变被认为会引起环区畸变,从而迫使稳定螺旋发生全局重排,使核心结构呈现类似变性态的特征。
在上述结构特征中,与该研究最为相关的是ROP蛋白模块化的七肽重复模式。作为一种刚性束状结构,且拥有大量几何特征已被精确表征的变体,ROP非常适合用于高阶蛋白结构的理性工程设计。然而,其天然长度不足以跨越单个IgG1抗体的两个结合位点。为探索七肽插入作为螺旋束延展方法的可行性,并作为构建更大尺度抗体复合体系的一步尝试,该研究将大肠杆菌ROP蛋白的长度从4.3nm延长至6.5nm,实现了50%的线性增长。文中系统报道了工程化设计流程以及由此获得的两种变体的晶体结构(图1)。尽管卷曲螺旋的从头设计方法已较为成熟,但该研究选择从结构和稳定性已被充分验证的ROP蛋白出发,以最大限度地保持其稳定性和几何精确性。工程策略包括首先引入色氨酸以实现精确定量,随后插入四个七肽重复,并在核心位置引入新的苯丙氨酸位点。实验结果验证了该设计思路的可行性,并表明延长后的蛋白保持良好稳定性,具备进一步工程改造和应用的潜力。
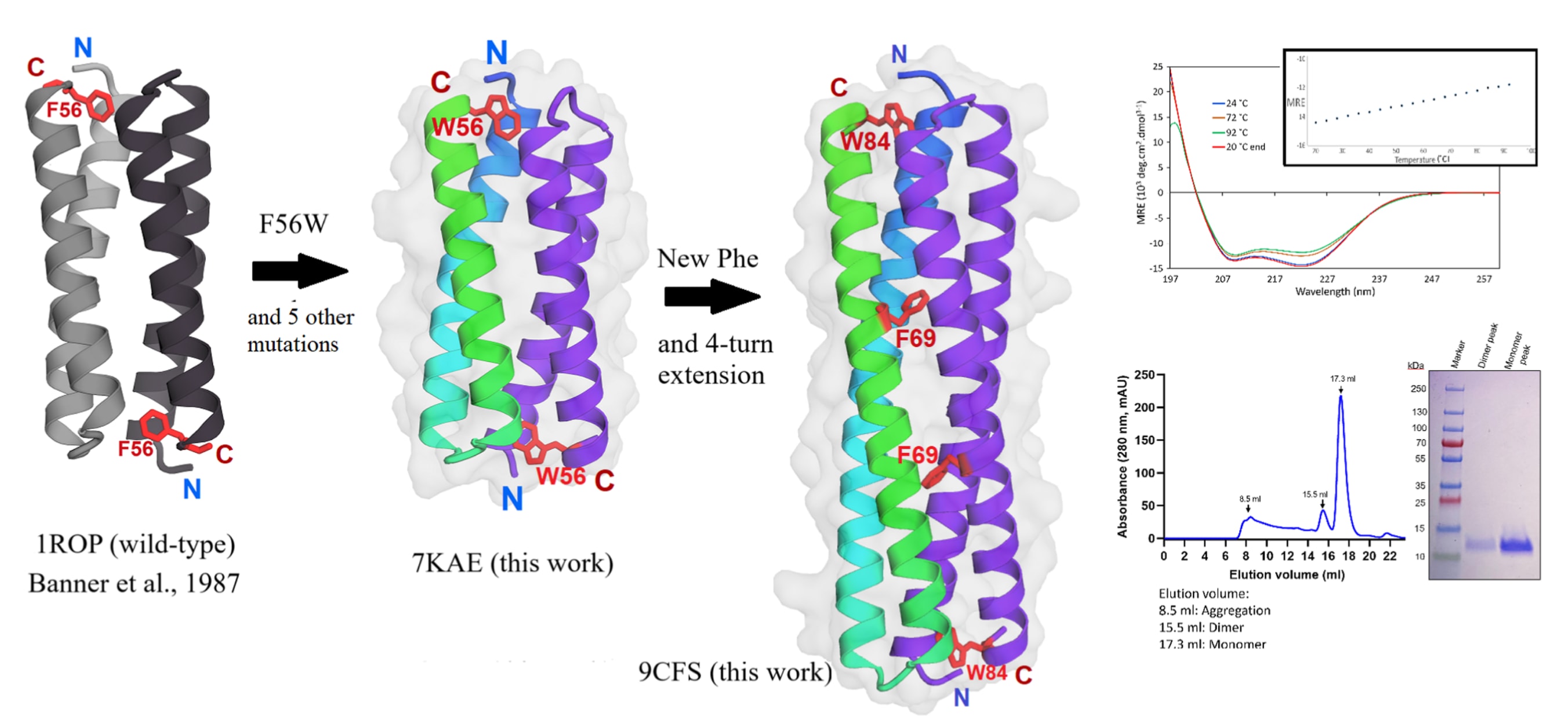
图1|图形化总结。 该图概述了在构建7KAE和9CFS过程中所采用的整体结构改造策略。图右侧展示了相应的生物物理表征结果,其中右上角的圆二色谱结果表明,9CFS蛋白具有明显的α螺旋构象,并在升温至92°C时仍保持稳定,其热变性过程具有可逆性。右下角给出了体积排阻色谱和SDS-PAGE分析结果,显示样品具有较高纯度。用于结构解析的晶体来源于体积排阻色谱中主要洗脱峰对应的蛋白组分。
2 材料与方法
2.1 实验与技术设计
图2概述了整体的工程化设计流程,该流程由三个连续步骤组成。每一个步骤均在设计标准的约束下,反复结合pymol、molprobity和rosetta等工具,对候选突变进行建模与分析,以确保结构合理性与稳定性。在第一步中,选择野生型结构1ROP作为起始模型,在对称二聚体的蛋白核心中引入一个色氨酸残基,使每个二聚体包含两个色氨酸。该构建体随后进行表达并成功结晶,获得了晶体结构pdb:7KAE。第二步为蛋白长度的实际延展设计,该过程在计算机模拟中完成,通过七肽重复复制对结构7KAE进行延长。在此过程中,持续进行序列与结构的迭代优化,以消除原子间的空间冲突并缓解不利的相互作用。第三步在已延长的蛋白结构基础上进一步引入一个苯丙氨酸残基,并配合额外的序列精修。最终获得的蛋白被成功表达并结晶,其晶体结构解析为pdb:9CFS。
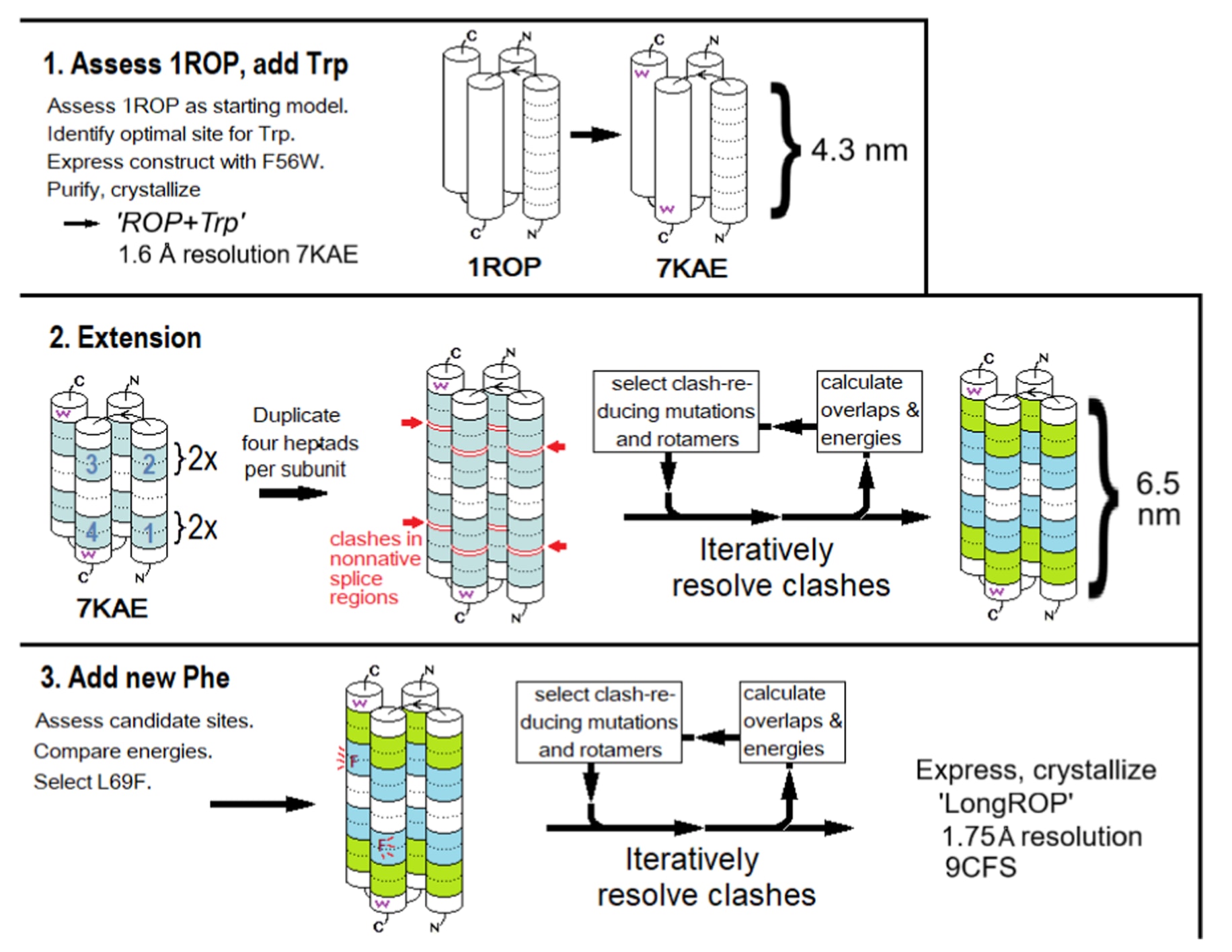
图2|技术设计流程。 第一部分中,选取初始结构模型,并在引入一个色氨酸残基以增强定量能力的同时,结合另外五处突变,构建得到中间结构pdb:7KAE。第二部分在7KAE结构基础上进行长度延展,并通过序列差异化处理以消除结构冲突,其中“冲突”不仅包括不利的空间位阻,还涵盖静电排斥和疏水性不匹配等相互作用。第三部分在延长后的结构核心中引入一个苯丙氨酸残基,并配合进一步的序列优化。最终设计得到的蛋白成功表达,并通过衍射实验解析至1.75Å分辨率,其晶体结构编号为pdb:9CFS。
2.2 引入色氨酸及另外五处突变
为提高紫外吸收能力以实现精确定量,在不牺牲蛋白稳定性和溶解性的前提下,引入一个色氨酸残基。野生型ROP蛋白中含有两个可作为候选替换位点的苯丙氨酸,分别位于第14位和第56位。晶体结构显示,第14位苯丙氨酸部分朝向溶剂,而第56位苯丙氨酸则紧密嵌入蛋白核心。由于色氨酸的吲哚环体积更大,若直接在56位引入色氨酸,将与相邻的半胱氨酸侧链产生明显的空间位阻。为消除该冲突,引入了补偿性突变C52A。
野生型蛋白中含有两个半胱氨酸残基,均位于拓扑学定义的核心a位点,因此将二者均替换为丙氨酸,以避免半胱氨酸化学反应性带来的潜在问题。已有研究表明,半胱氨酸会影响蛋白折叠动力学,但其替换并不会显著扰乱整体结构。建模结果显示,这些突变会在蛋白内部形成小尺度空腔,但在该研究设计中,消除半胱氨酸氧化敏感性的收益被认为超过了由此带来的轻微失稳风险。
最终的F56W突变体序列设计还在第16至20位残基区间引入了三处突变,将RSQTL替换为QNQTQ,以改善蛋白的溶解性、稳定性和结晶能力。这三个位置分别对应经典七肽重复中的e、f和b位点(见图4)。将精氨酸替换为谷氨酰胺旨在降低表面构象熵,丝氨酸被替换是因为其在α螺旋中出现频率较低,而亮氨酸的替换则源于其在野生型结构中暴露于溶剂环境,不利于溶解性。
2.3 蛋白长度延展的设计
野生型ROP蛋白由四个七肽重复构成。为实现结构延展,在每一条螺旋中插入两个额外的七肽重复。该设计基于这样一种假设,即标准α螺旋每7个残基大约完成两次旋转,在相位上近似重复,因此七肽可作为一种可插入的模块,即便在多螺旋束结构中亦适用。由于目标是保持蛋白的稳定性和力学刚性,所有新的连接界面和拼接位点均需避免明显的空间位阻,并在能量上处于放松状态。鉴于四螺旋束的对称性,为在整体结构上增加四个螺旋圈数,必须在序列中的四个不同位置分别插入七肽模块。由此,蛋白序列长度增加了
在通过复制一个包含两个螺旋圈的片段实现初步延展后,进一步开展了多轮序列差异化与优化。利用Molprobity识别空间位阻,并结合Pymol在常见旋转异构体范围内评估可能用于缓解冲突的突变。此处所称的“冲突”不仅包括空间位阻,还涵盖静电排斥和疏水性不匹配等能量不利因素。能够完全或部分缓解冲突的突变会被作为候选,并进一步在相邻位点引入新的突变进行评估。所有突变位点汇总见图4。初始阶段,显著的冲突主要集中在相邻重复模块的非天然拼接界面附近,对应于85个残基序列中的第14、34、54和73位区域。随着这些冲突被逐步消除,新的冲突往往在邻近区域出现,使突变区域逐渐向外扩展。通常需要进行10至15轮迭代,才能获得无明显冲突的候选结构,并进一步使用Rosetta进行详细的能量评估。候选方案同时根据亲水性和电荷分布进行筛选。该过程之所以相对高效,得益于ROP蛋白结构的高度简洁性以及已有的高分辨率结构先例。大多数侧链在拓扑上可清晰区分为核心、表面或半埋藏位置,且除表面位点外,其余位置在空间上均受到较强限制。冲突严重程度的评估同时考虑了侧链与主链的键合距离。由于蛋白几乎完全由α螺旋构成,突变设计倾向于选择有利于螺旋形成的残基,其优先级依据螺旋倾向性排序为EMALK > FQWIV > DHRTS > CYNPG。综合考虑螺旋倾向性以及核心与表面位点在疏水性上的差异后,每个位点通常仅剩少数可选残基。多轮迭代最终促成了一些协同补偿突变簇的形成。Rosetta用于对最有前景的候选结构进行能量最小化并比较其能量水平,同时对最初完全相同的重复区域赋予序列差异化的优先权,使蛋白序列逐步演化为全长范围内的唯一序列。
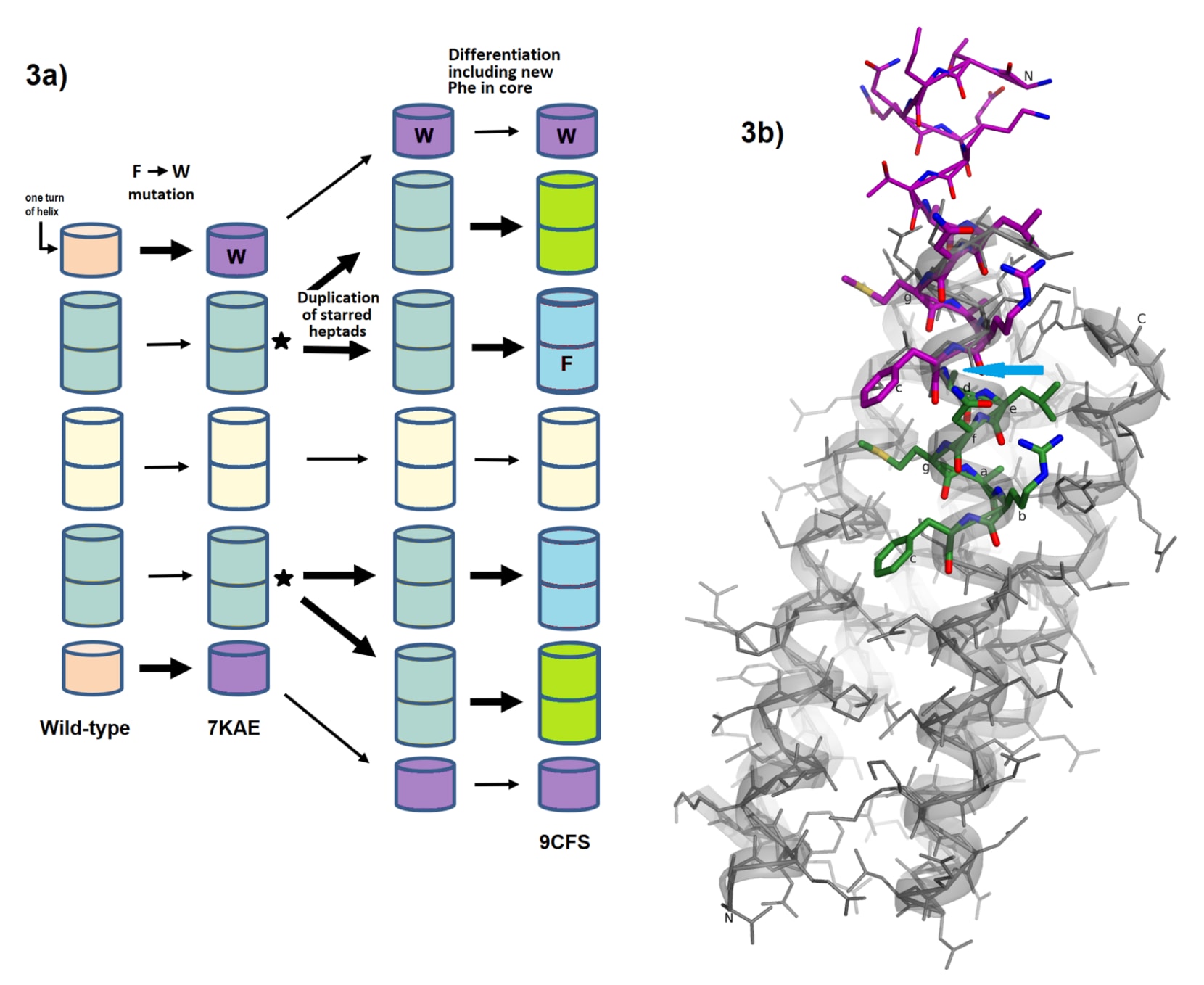
图3|延展型ROP设计中的关键步骤。 (a)示意图展示了在C端螺旋上实施的主要结构改造,这些螺旋包含苯丙氨酸和色氨酸位点,其余螺旋以相同方式并行改造。图中每一段圆柱体代表一个α螺旋圈,每一步设计均包含多轮基于pymol、molprobity和rosetta的结构分析与优化。(b) 展示了束状结构中单个N端的延展机制。由第8至14位残基组成的七肽序列ALNMARF以绿色标示,该图以7KAE结构为例,但相关残基在野生型1ROP中保持一致。紫色片段表示将第1至14位残基整体向上平移一个七肽长度后得到的精确拷贝。自绿色七肽起,随着结构延展,残基编号按每次增加7个递增。在重复片段之间的拼接位置附近,如箭头所示,容易出现非天然的相邻相互作用和潜在冲突,这些冲突既可能发生在单条螺旋内部,也可能出现在不同螺旋之间。拓扑学位置标注方式与文献中一致。通过类似的七肽复制和平移操作,束状结构中全部8个螺旋端均得到了延展。随后通过进一步优化,将第14位苯丙氨酸替换为谷氨酰胺,并将第21位苯丙氨酸替换为谷氨酸,相关突变亦见图4。

图4|展示了1ROP、7KAE和9CFS的氨基酸序列及其对应的残基编号。 发生突变的残基以星号标示。序列中重复的七肽结构被特别强调,其中字母“x”表示序列的延伸部分。拓扑位置的标注方式与文献中采用的定义一致。同时还给出了中间体蛋白Imww的序列,该序列位于最初延伸蛋白与最终序列之间。
2.4 重新引入苯丙氨酸
在同时追求提高序列差异性和稳定蛋白核心这两个目标的前提下,对引入新的苯丙氨酸位点进行了系统评估。尽管野生型ROP蛋白中原本含有两个苯丙氨酸残基,其中一个已被替换为色氨酸,另一个位于第14位的苯丙氨酸由于处于溶剂暴露位置而被替换为谷氨酰胺,从而使延长设计阶段的蛋白不再含有苯丙氨酸。为此,对所有位于蛋白内部的苯丙氨酸替换方案进行了考察,仅考虑标准旋转异构体,并排除了会与主链或Cβ原子产生空间位阻的候选位点。对初步筛选出的有利候选位点,进一步允许在其邻近残基处引入补偿性突变进行综合评估。该过程最终确定第69位亮氨酸替换为苯丙氨酸是最优方案,该位点在野生型和7KAE结构中对应第48位亮氨酸,并且处于一个由多处协同突变组成的局部突变簇之中。Rosetta计算显示,在引入L69F突变前后,模型的总能量分别为-577kcal/mol和-590kcal/mol,表明该突变簇并未导致蛋白失稳。鉴于理论能量计算可能存在偏差,且核心区域的扰动通常容易引发稳定性下降,对该构象进行了更为细致的几何分析。建模结果显示,新引入的苯丙氨酸在核心中具有良好的堆积方式,因此将该突变作为一种工程权衡予以保留,认为其在潜在稳定性提升和序列多样性方面的收益超过了可能带来的失稳风险。
2.5 质粒与蛋白制备
为了便于蛋白纯化,起始甲硫氨酸被替换为甘氨酸,并在N端延伸加入MGHHHHHH-序列。同时,C端被截短至第57位甘氨酸,因为在多数包含该区域的晶体结构中,其后6个野生型残基通常呈现无序状态。
7KAE基因由Genscript合成并克隆至pET-15b质粒中。按照生产商的建议,将10ng质粒直接转化至Bl21 DE3感受态细胞中。随后取200μL转化产物涂布于含100μg/mL氨苄青霉素的LB琼脂平板上,从中挑取单个菌落接种至含相同抗生素浓度的100mLLB培养基中,在30°C、225rpm条件下振荡培养16h。过夜培养液用于接种两个4L挡板摇瓶,每个摇瓶中含1.5L加入100μg/mL氨苄青霉素的LB培养基。培养在37°C、190rpm条件下进行,并持续监测600nm处的光密度。当OD600达到1.5时,加入IPTG至终浓度1mM以诱导蛋白表达,随后将培养温度降至30°C并继续振荡培养过夜。次日以2500g离心20min收集菌体,共获得17g湿重细胞沉淀,并在-80°C条件下冷冻保存以备后续处理。冷冻的细胞沉淀经解冻后,以每克细胞加入5mLPBS缓冲液进行重悬,缓冲液组成为10mM磷酸钠、120mM氯化钠,pH7.2。样品随后通过Constant Systems Ltd型号CF1的细胞破碎仪处理两次。加入终浓度为1mM的苯甲基磺酰氟以抑制蛋白降解后,以7000g离心1h获得澄清的上清液。该上清液被加载至预先用PBS平衡的5mLHisTrap亲和层析柱中,随后用含50mM咪唑的PBS洗脱五个柱体积,最后使用含400mM咪唑的PBS进行洗脱。洗脱液经Amicon Centriplrep装置(分子量截断3kDa)进行10倍浓缩并置换至PBS缓冲液中。随后将浓缩样品上样至预先用PBS平衡的400mLSephacryl S-100 HR凝胶过滤柱进行分离,收集吸收峰对应的级分并合并。合并样品在25mM Tris、150mM NaCl、pH7.5缓冲液中,以100倍体积进行两次过夜透析。最终样品使用3kDa分子量截断的Amicon装置浓缩至11mg/mL。蛋白9CFS的制备方法与上述流程基本一致,不同之处在于使用的Centriprep分子量截断值为10kDa。
2.6 生物物理表征
圆二色谱的波长扫描与温度扫描使用Applied Photophysics公司的Chirascan圆二色谱仪完成。圆二色谱数据记录的波长范围为190–260nm,光谱带宽为1nm,每个数据点的采集时间为1s。温度熔解实验在20°C至92°C范围内进行,升温速率为1°C/min,并通过监测222nm处椭圆率的变化来跟踪构象变化。蛋白样品以0.25mg/mL的浓度溶解于含90mM NaF、10mM NaCl和25mM Tris,pH8.0的缓冲液中,并置于光程为0.1cm的比色皿中。完成温度扫描后,样品被冷却回室温并重新测量,结果证实蛋白的热变性过程具有可逆性。蛋白9CFS的分子尺寸分析通过体积排阻色谱完成,使用Superdex 200 Increase 10/300 GL色谱柱,流速为0.4mL/min,进样体积为500μL。SDS-PAGE分析所用凝胶为4–20%的梯度胶。
2.7结构测定与预测
针对两种蛋白变体,纯化后的样品在约300种不同的化学条件下进行了结晶筛选,并在多轮实验中对晶体生长条件进行了重复验证和优化。最终获得的结晶条件为:7KAE使用28%聚乙二醇400、300mM NaCl、100mM NaHepes,pH7.5;9CFS使用200mM磷酸钠、30%聚乙二醇300,pH5.2。单晶体经采集后迅速浸入液氮中进行冷冻,并在低温条件下完成数据采集。7KAE的数据采集于Argonne国家实验室先进光子源的19-BM光束线完成,9CFS的数据采集于Brookhaven国家实验室NSLS2的17-ID-1光束线完成,分别获得了1.6Å和1.75Å分辨率的衍射数据。两种蛋白结构均通过分子置换方法求解。对于9CFS,搜索模型由假设结构出发,去除了发夹环结构、末端区域以及较长的表面侧链。随后,在差异电子密度图的引导下,使用CCP4软件包以迭代方式重建被省略的结构部分,并加入水分子,最终获得并提交了7KAE和9CFS的结构模型。在蛋白结构附近观察到一个明显的电子密度峰,该峰位于His58和His72的咪唑环约2.0Å处,并距Glu54的羧酸基约2.2Å。这三个残基均不存在于野生型蛋白或7KAE中。该位点的配位方式类似于二价过渡金属离子,例如镍。鉴于蛋白在纯化过程中通过镍亲和柱进行富集,并且结晶条件中未使用除钠以外的重金属,该电子密度峰极有可能对应一个在结晶过程中被保留下来的镍离子,因此在结构模型中将其建模为镍。该金属离子的存在并未对蛋白的折叠或核心结构产生明显影响。此外,9CFS的结构还使用AlphaFold 2.3版本通过ColabFold在线服务器进行了预测,整体置信度指标pLDDT为98。尽管该预测结构未用于实验结构的求解,但结果显示,AlphaFold预测的模型能够产生与实验中所用模型相似的分子置换解。
3 结果
由四个段落组成,主要围绕工程化蛋白结构的关键特征展开。这些特征基于晶体学观察结果加以描述,同时结合了螺旋束延伸过程中获得的实验发现,从结构层面阐明了设计策略对蛋白折叠与组装方式的影响。
3.1 引入的色氨酸
ROP+Trp变体的晶体结构(PDB 7KAE)显示,新引入的色氨酸位点与Glu5的羧酸基团发生堆叠作用,其中Trp56的吲哚环指向蛋白内部核心,其氮原子则朝向溶剂暴露(图5)。野生型蛋白与7KAE之间以α-碳为基础计算的均方根偏差为0.9Å。结构叠合结果表明,该氨基酸替换并未对局部主链构象产生明显扰动,其差异处于约0.2Å的坐标误差范围内。两个由半胱氨酸突变为丙氨酸的位点均在结构中形成了类似巯基体积的空腔,其中C52A位点的空腔部分被Trp56的吲哚环所填充。在7KAE结构中,两条多肽链呈现出轻微的构象差异,其56个α-碳之间的均方根偏差为0.4Å。尽管主链和核心侧链在旋转异构体层面保持一致,但Phe14的构象表现出明显的不对称性,两条链中的苯丙氨酸侧链分别采用了不同的旋转构象。ROP+Trp在溶液中的行为与野生型蛋白相似,并且能够形成具有足够衍射质量的晶体,从而获得了分辨率为1.6Å的7KAE晶体结构。
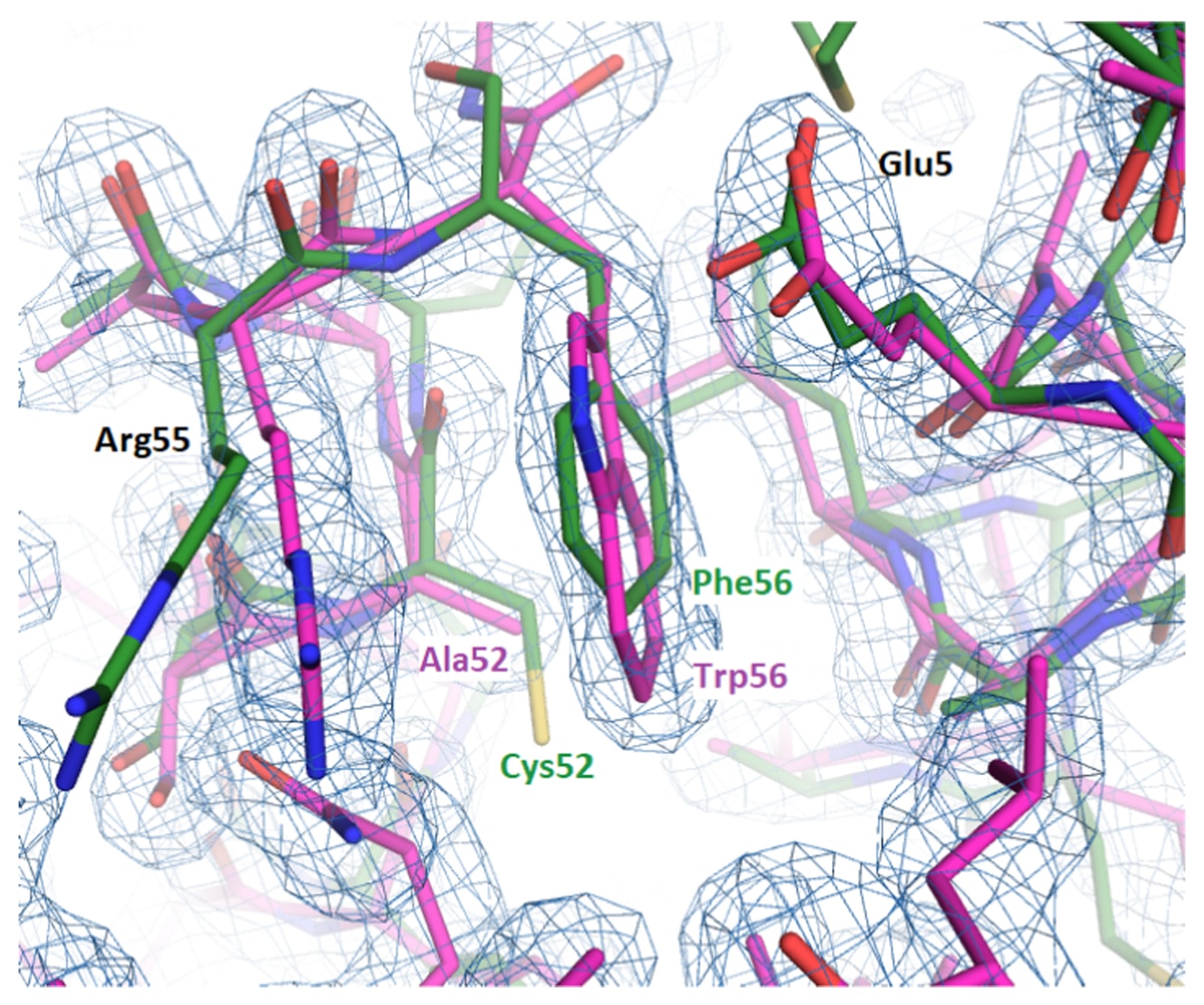
图5|展示了Phe56被Trp替换后的结构特征。 图中以洋红色显示7KAE结构中引入的色氨酸及其周围区域,野生型结构以绿色叠加显示。同时给出了7KAE的电子密度图,等高线水平为1.8σ。相邻的Cys52到Ala的突变用于补偿色氨酸体积增大所带来的空间占据变化。
3.2 将ROP延长50%
将由56个残基组成的7KAE蛋白延长至85个残基是通过复制4个七肽重复单元实现的,从而在序列的4个不同位置共增加了28个残基。被复制的片段大致位于螺旋束末端与中心二重轴之间的中部区域。最初复制得到的序列彼此完全相同,随后通过多轮迭代修饰,使这些区域在结构上具有唯一性,从而促进二聚体的正确组装。经过多次迭代,该过程将第8–21位残基从ALNMARFALNMARF逐步演化为最终9CFS序列中的ALQMAKQIKQQAQE。序列优化覆盖了整个蛋白,最终约25%的位点发生了替换,尤其集中在表面残基。在最终结构中,主链以及核心侧链均呈现良好的有序性,而有4个表面侧链共12个非氢原子未能在电子密度中观察到,表现为无序状态并未包含在9CFS模型中。突变侧链的χ1旋转异构体总体上保持一致,并与已知统计规律相符。该结构与AlphaFold预测模型高度一致,在170个Cα原子上的RMSD为0.8Å。在该左手性卷曲螺旋束中,每条螺旋在12个螺旋转角内绕中心轴旋转约120°(图6)。

图6|展示了沿分子轴方向观察的延长ROP中一条多肽链的投影图。 碳原子按照序列位置由蓝色渐变至红色着色,显示每条螺旋在螺旋束的超螺旋结构中绕中心轴旋转约120°,且这种旋转沿整个螺旋束长度连续而平滑。图中特别强调了两个新引入的芳香族残基Phe69和Trp84,白色圆圈标示分子轴的位置。尽管在该投影视角下苯丙氨酸与色氨酸看起来彼此接近,但实际上二者之间的距离约为1.5nm,约占整个螺旋束总长度的三分之一。在该视图中,多肽链的N端和C端位于观察者近端,而位于序列中部的环区则以黄绿色显示,位于远端。
由于在设计中对残基选择施加了限制,在表面位置强烈偏好EKQ,在核心位置偏好MALF,最终蛋白的氨基酸组成呈现出非典型特征,其中谷氨酰胺含量显著升高,达到13%,而在全局统计中通常约为4%。野生型ROP不含脯氨酸、缬氨酸和色氨酸。设计过程中引入了色氨酸和脯氨酸(位于蛋白的发夹转角处),去除了所有半胱氨酸、丝氨酸和苯丙氨酸,随后又重新引入了一个新的苯丙氨酸位点。基于螺旋倾向性的加权设计使最终序列富含丙氨酸、谷氨酸、谷氨酰胺和赖氨酸。
3.3 苯丙氨酸的重新引入
7KAE结构中仅包含一个苯丙氨酸,即野生型中保留的Phe14。在延长蛋白的设计中,由于该位点暴露于溶剂环境,该残基被谷氨酰胺替换,从而使蛋白中不再含有苯丙氨酸。随后评估了是否可以重新引入一个新的苯丙氨酸位点,以在保持蛋白稳定性和溶解性的同时,为延伸的螺旋束区域生成非重复序列。基于Pymol和MolProbity的分析,在若干相互接触侧链需要补偿性突变的背景下,Leu69被确定为最有利的引入位点。如图7a所示,新引入的芳香侧链在该拓扑学上的“d”位点被良好地容纳,其chi1旋转异构体得以保持,且主链未出现明显扰动。图7b进一步显示,该新的苯环与周围核心区域紧密贴合。唯一相邻的空腔由水分子104占据,该水分子与Ala19和Ala66的羰基形成氢键。值得注意的是,1ROP结构中也存在一个非常相似的核心邻近水分子位点,即水分子79,其由对应的Ala12和Ala45配位。这些参与水分子配位的丙氨酸残基均位于七肽重复单元中的“a”位置。
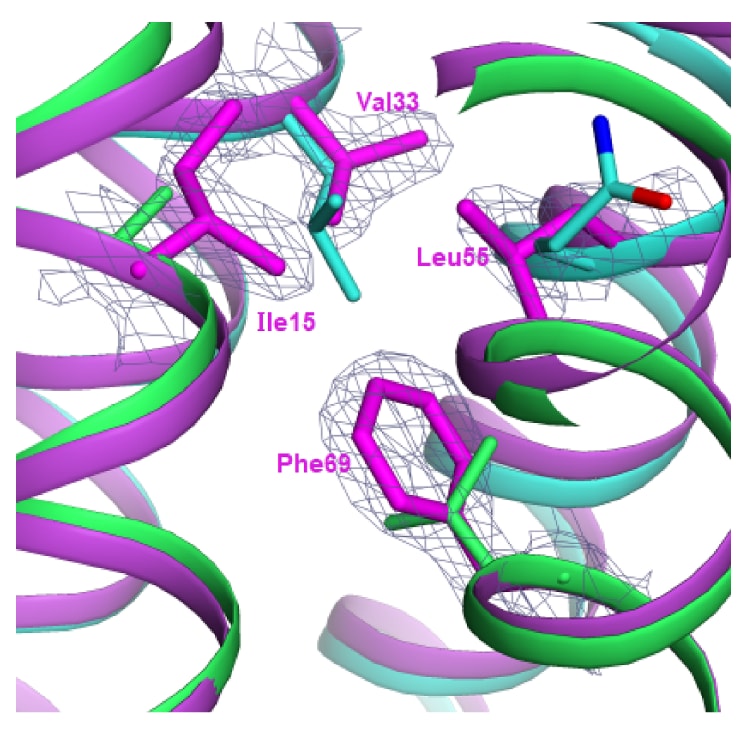
图7a|展示了晶体结构9CFS中围绕新引入苯丙氨酸位点形成的突变簇,该位点位于蛋白核心区域。 Phe69在9CFS中取代了1ROP和7KAE中的Leu48,其体积增大通过相邻位点的补偿性突变得以缓解,从而实现了局部核心结构的重新堆积。为便于观察,图中仅显示了四个突变位点,分别位于四条螺旋上。由于在序列中插入了七肽重复单元,9CFS中的残基编号相较于1ROP和7KAE中对应位置均增加了7的整数倍。图中以洋红色显示9CFS结构,并给出了等高线为1.8σ的电子密度图;7KAE结构则以绿色和青色叠加显示。
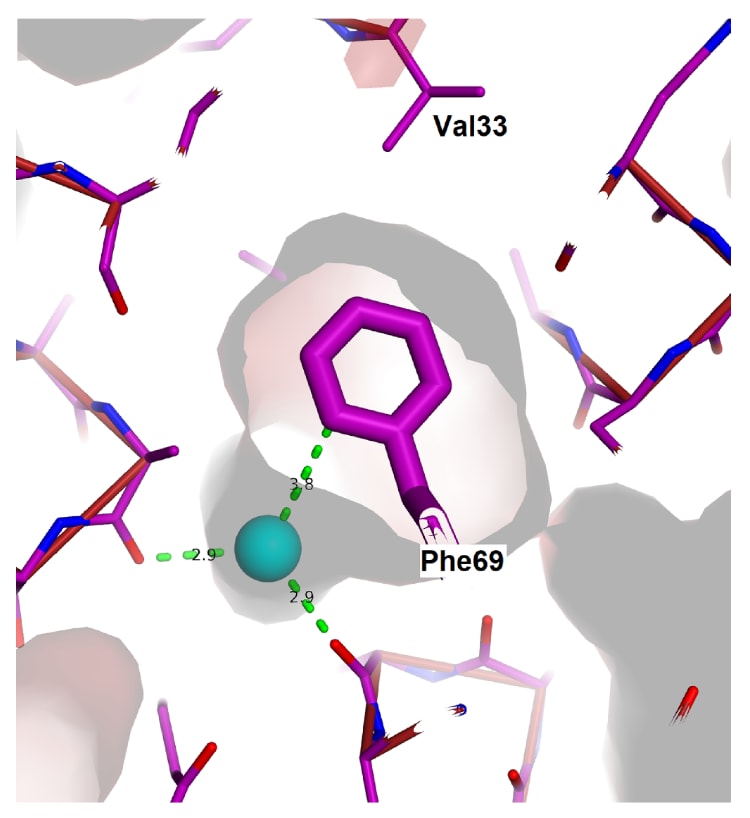
图7b|展示了Phe69及其相邻的核心水分子。 周围蛋白的范德华表面显示,该苯基与局部结构之间形成了紧密贴合。苯环附近唯一存在的空腔由一个水分子占据,该水分子位点在1ROP结构中同样可以观察到,即使当时尚未引入苯丙氨酸。这一现象表明,Phe69的引入并未对蛋白核心结构造成扰动。
3.4 协同突变簇
在从ROP+Trp到LongROP的设计过程中,有两个彼此独立的区域在多轮循环中逐渐形成了协同突变簇,并最终收敛至稳定的最终序列。第一个区域位于复制七肽之间的非天然拼接区,第二个位于新引入的Phe69位点周围。在这两个区域中,最初的空间冲突通过一系列部分补偿性的突变逐步得到缓解,这些突变沿着螺旋结构扩散,覆盖约两个螺旋转角的范围,并逐渐实现收敛。这一过程因主链几何结构被精确限定而显著简化,这种几何约束也使核心侧链与表面侧链之间具有较为清晰的区分。此外,突变在设计中被强烈引导至有利于α螺旋形成的残基类型,使得每个位点可选择的侧链种类有限,通常仅对应少数可能的旋转异构体。通过多轮突变建模与空间冲突评估,所有冲突最终被消除,并获得了稳定的最终序列。
4 讨论
蛋白工程的两个常见目标是提高物理稳健性,例如溶解性或稳定性,尤其是酶的热稳定性,以及改善与关键配体之间的结合或催化能力。与之正交的发展方向上,出现了两类广泛适用的方法:其一是体外定向进化方法,例如随机DNA文库合成结合噬菌体展示进行筛选;其二是基于实验确定的结构与功能关系所进行的理性设计,并辅以利用结构信息模拟定向进化的软件方法。
当前可用的结构信息已包括存储于PDB中的海量经验证的三维分子结构数据,这些数据支撑了Rosetta和AlphaFold等强大的从头折叠与结构预测方法。这两类通用方法均通过多轮迭代逐步优化目标性质,适用于提高熔解温度Tm或降低解离常数Kd等常见工程目标。抗体是工程化程度最高的蛋白类型之一。随着结构免疫学的发展以及抗体制备方法的改进,利用适当工程化的单克隆抗体治疗多种疾病已成为现实。然而,在表征抗体构象变化方面仍然存在不足,尤其是在三维空间中定量描述其扭转与弯曲幅度方面。由于双价结合功能及下游生物信号传导均受整体三叶结构构象的影响,构象测量技术对于引导柔性蛋白药物进入有效构象具有重要意义。该研究并未聚焦于高度柔性的抗体体系,而是选择了大肠杆菌中的ROP蛋白,该蛋白为刚性的四螺旋束结构。该项目的目标是将该螺旋束从天然长度4.3nm延长50%至6.5nm,以作为更大组装体系中的组成元件。尽管热稳定性并非明确的设计目标,但在延长变体中保持野生型蛋白的稳定性和溶解性仍然至关重要。作为第一步,构建了中间体ROP+Trp,其目的在于引入色氨酸以增强紫外吸收,从而实现精确的蛋白定量。进一步获得LongROP的工程化过程具有蛋白特异性,主要通过在序列中四个选定位置插入两个螺旋转角的七肽单元来实现。该策略在序列中引入了非天然拼接点,并产生局部空间冲突,这些问题通过逐步消除冲突并优化序列得以解决,最终获得了分辨率为1.75Å的晶体结构9CFS。圆二色谱结果表明,该延长结构保持螺旋特性,并在高达92°C的条件下仍然稳定,说明螺旋束可以在保持稳定性的前提下实现平行延伸。这一结果引出了该过程是否可以进一步重复以及可延伸极限的问题。类似的策略可能适用于其他螺旋束结构的长度扩展。延长后的ROP结构具有刚性且几何参数精确可控的特征,可作为一种通用的纳米尺度工具,尤其适用于抗体构象测量领域,并可通过进一步修饰作为功能性连接的支架或构建模块。