Nature 2026|多组学解析人类海马神经发生:从成年期到衰老,再到阿尔茨海默病
今天介绍的这项研究发表于 Nature 。作者结合 单核转录组测序(snRNA-seq) 与 单核染色质可及性测序(snATAC-seq),对来自五个独立队列的 355,997 个海马细胞核 进行了多组学整合分析,在成人脑中系统识别出 神经干细胞(NSC)、神经母细胞(neuroblast) 以及 未成熟颗粒神经元 等神经发生谱系细胞。研究发现,神经发生过程中的失衡更多体现在 染色质可及性差异(DAR) 的重塑,而不仅仅是 mRNA 表达水平的变化。在 临床前阶段(PCI) 即可观察到神经发生相关细胞中 开放染色质的早期改变,并在 阿尔茨海默病(AD) 进程中进一步加剧。与认知衰退个体相比,超级老年人(SuperAgers) 展现出区别于普通老年人的 神经发生韧性(neurogenic resilience)。此外,研究还提示 星形胶质细胞(astrocytes)与 CA1 神经元 的网络重塑可能共同影响衰老过程中认知功能的维持或下降。在调控网络层面,作者进一步系统比较了不同诊断组中的 增强子驱动调控模块(eRegulon),并结合 CellChat 的配体—受体互作分析,将 星形胶质细胞、CA1 神经元与神经发生细胞 整合为一个可计算的细胞通信网络。结果提示,兴奋性突触完整性以及谷氨酸能信号传递 可能是区分 成功衰老(successful aging) 与 认知功能恶化 的关键机制。

获取详情及资源:
- 📄 论文:https://doi.org/10.1038/s41586-026-10169-4
- 🧬 数据:GEO:GSE268609
0 摘要
人类海马在成年期是否仍持续发生神经发生长期存在争议,其与认知的关系也不清楚。近期研究已证实存在持续增殖的祖细胞与未成熟神经元,并观察到阿尔茨海默病(AD)中未成熟神经元减少。然而,这些细胞的来源,以及调控神经发生及其功能的分子网络仍缺乏解释。该研究分析来自不同队列的人类海马尸检样本,包括记忆完整的年轻成人、无认知障碍的老年人、记忆能力异常出色的超级老年人、处于临床前中间病理阶段的个体,以及AD个体。作者通过单核多组学测序(snRNA-seq与snATAC-seq)对海马样本中的355,997个细胞核进行剖析,识别出神经干细胞、神经母细胞与未成熟颗粒神经元。神经发生的紊乱主要与染色质可及性的改变相关。进一步基于转录因子与靶基因特征的比较发现,临床前AD个体的神经发生细胞已经出现早期染色质可及性异常,而在AD样本中更为显著。超级老年人表现出不同于其他队列的神经发生特征,可能反映一种“韧性特征”。此外,星形胶质细胞与CA1神经元谱系的改变共同影响衰老海马的认知功能。总体而言,该研究提出一套能够区分衰老过程中认知韧性与认知衰退的海马多组学分子特征。
1 引言
在啮齿动物中,齿状回颗粒下层(subgranular layer)的神经干细胞(NSC)生成新神经元的转录与表观遗传机制已较为清楚。海马神经发生通过将未成熟神经元招募进记忆回路,参与学习与记忆形成。随着啮齿动物衰老,神经发生下降;在AD小鼠模型中也会受损,并与记忆缺陷相关。相比之下,人脑中神经发生的走向、调控机制及其在认知中的作用仍知之甚少。
成年期人类海马是否存在神经发生在近年引发持续争论,主要原因包括使用的物种特异性标志物不一致、样本处理差异、细胞注释与计算分析限制等,同时未成熟神经元与抑制性神经元的分子特征重叠也会干扰判定。基于单核RNA测序(snRNA-seq)的工作已证实成年人人脑存在未成熟神经元,并观察到AD中未成熟神经元减少;此外,成年脑中的一部分祖细胞显示出持续增殖的迹象。然而仍有几个关键空白:第一,神经发生的表观遗传基础尚不清楚,明确这一点有助于理解不同个体神经发生能力的差异;第二,支配成人海马神经发生的基因调控网络(GRN)仍未知;第三,神经发生与人类认知功能之间的联系,以及从健康衰老向AD过渡的临床前阶段是否已出现神经发生受损,仍缺乏证据。相反,记忆表现异常出色的人群,其神经发生特征也几乎未被系统刻画。
为回应这些问题,作者对人类海马尸检样本开展单核多组学分析,联合单核转录组测序(snRNA-seq)与单核染色质可及性测序(snATAC-seq),覆盖五类队列:认知完整的年轻成人(YA)、认知表现符合年龄水平的老年人(HA)、可能从HA过渡到AD的临床前中间病理个体(PCI)、AD个体,以及超级老年人(SA,指80岁及以上且情景记忆表现不低于50~59岁人群的个体)。
2 神经发生的调控网络
为建立成人海马神经发生的调控框架,作者首先分析了年轻成人(YA)队列:8名20~40岁、认知完整的供体,共计85,977个细胞核。为保证细胞注释的稳健性,作者采用基于机器学习的标签转移策略,使用scVI框架中的scANVI把两个既有人类脑scRNA-seq数据集的标签迁移到该研究的snRNA-seq数据上,一个来自人类发育期前脑,另一个来自成人海马数据集。基于snRNA-seq的无监督聚类在海马中识别出12类细胞类型,并包含神经发生相关的神经母细胞与未成熟神经元。二维UMAP可视化显示,未成熟神经元位于成熟颗粒神经元簇的外缘;而神经母细胞簇与成熟少突胶质细胞(mOL)簇部分重叠。对神经母细胞与mOL进行差异表达基因(DEG)与通路分析,得到4,166个DEG与169条通路,且均在神经母细胞中上调;其中80条通路与树突、轴突、突触后致密区与神经递质传递等过程相关。为解释两个簇在UMAP上的视觉接近性,作者进一步对照单细胞转录组人脑图谱中的“代理标志物(proxy)”,发现与少突胶质细胞相关的MAG与MOG在神经母细胞中也有表达,但水平低于mOL,这可能部分解释二者在嵌入空间的邻近,而其基因表达谱仍然清晰可区分。
在确定神经发生谱系与其发育方向时,作者对星形胶质细胞、神经母细胞、未成熟神经元与成熟颗粒神经元簇进行RNA velocity分析,并用“潜在时间(latent time)”刻画分化进程。结果显示,机器学习识别出的未成熟神经元潜在时间低于成熟颗粒神经元;此外还存在两个潜在时间高于星形胶质细胞、但低于未成熟神经元的亚簇,其中一个可验证为神经母细胞簇。另一个亚簇与星形胶质细胞相比出现766个DEG(671个上调、95个下调);其通路分析显示,65条通路中有25条与神经元发育相关,包括轴突发育、郎飞结、轴突初段、生长锥、轴突导向、树突棘与突触后致密区等,因此该亚簇被定义为神经干细胞(NSC)。综合RNA velocity的方向性流动,作者观察到从NSC指向一个星形胶质细胞亚簇,并进一步经由未成熟神经元走向神经母细胞,最终到达成熟颗粒神经元的连续轨迹,从而支持成人海马中存在神经发生的发育序列。
与啮齿动物报道一致,人类NSC相较神经母细胞与未成熟神经元表现出更高的“干性”代理标志物、以及更低的神经元标志物表达。更重要的是,snATAC-seq提供了对干性的正交证据:与多谱系潜能相关的区域在NSC中呈现更高的染色质可及性,而神经元成熟相关的代理标志物在神经母细胞与未成熟神经元中呈现更高的开放染色质水平。作者将该研究的神经发生特征与先前在齿状回观察到神经发生的研究进行比较,显示出较高一致性;同时把该特征应用到多个大规模全脑scRNA-seq数据集中,在“预期不应出现神经发生”的脑区中验证其特异性,从而进一步支持该特征能较好区分神经发生相关细胞。
在分子层面,作者比较不同细胞类型的DEG与差异可及区域(DAR)发现:NSC中的前列DEG与DAR在神经母细胞中下调,并在未成熟神经元中进一步下调;相反,神经母细胞的前列DEG与DAR在NSC中下调。部分基因在未成熟神经元中继续上调,而另一些则维持或下降,提示沿轨迹发生转录组状态切换。通路层面,β-catenin、基底外侧质膜等发育相关通路在NSC中富集,并在神经母细胞与未成熟神经元中下调;而未成熟神经元富集的通路更偏向突触功能与可塑性。对开放染色质区域的基序(motif)富集分析提示,NSC中最显著的基序来自STAT家族转录因子(如STAT3、STAT4、STAT5),以及PLAGL1与NFIB;而在未成熟神经元中,则更偏向RFX2、FOS–JUN、NFE2、MEIS2与PBX2等。这种差异支持从“维持干性与增殖”的调控因子逐步过渡到“驱动神经元分化与成熟”的调控因子。
由于同时具备配对的snRNA-seq与snATAC-seq,作者进一步用TF–peak–gene三元组方法与SCENIC+推断增强子驱动的调控网络(eRegulon),从而建立神经发生的GRN图谱。总体趋势显示,NSC中最强的调控互作在神经母细胞中下调,并在未成熟神经元中进一步下调;而NSC中不存在的互作在神经母细胞中轻度上调,在未成熟神经元中上调更明显。尽管互作强度随细胞类型变化,其上调或下调的方向在细胞类型间相对一致。不同细胞类型由不同的eRegulon网络主导:NSC中最显著的eRegulon包括RORA、RORB、SMAD1、ZNF98、SOX6、PRRX1、NFIA、GLIS3、BCL6与ETV6;神经母细胞中包括ZNF740、ZNF180、THRA、NFE2L1、NEUROD1、FEZF2、EGR1、EGR3、E2F1以及NRF1的抑制子;未成熟神经元中包括ZNF589、ZNF519、TFDP1、ONECUT2、MTF2、MTA3、GLIS1、E2F3以及SOX2与MXI1的抑制子。上述单核多组学分析共同给出了成人海马神经发生的多层次分子框架。
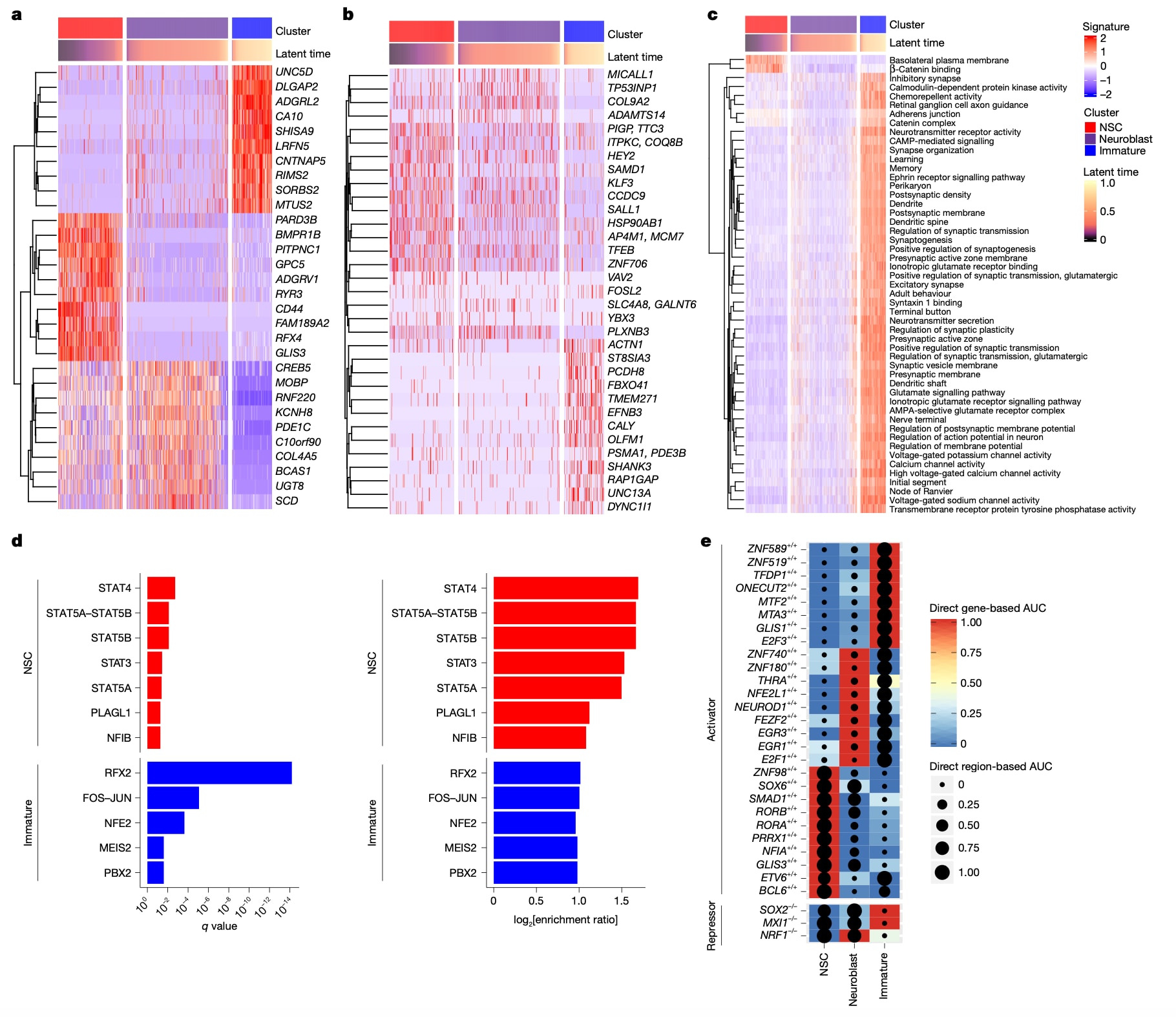
图1|成人脑中神经发生的分子网络。 a,YA样本中每类神经发生细胞的前10个差异表达基因(DEG)。b,YA样本中每类神经发生细胞基因启动子区域的前10个差异可及区域(DAR);标注基因对应存在重叠启动子的情况。前10个DEG与DAR分别按在所有显著差异(q<0.05)DEG或DAR中表达差异百分比的大小选取。c,基于神经发生相关DEG的通路特征:通路分析使用的DEG阈值为校正后P<0.01、log2FC>1且差异百分比>0.3;富集通路按FDR<0.05筛选,并对NSC与神经母细胞强调核内基因功能;未成熟神经元的通路筛选阈值为FDR<0.01且log2enrichment ratio>2。d,NSC与未成熟神经元中开放染色质增加区域的基序(motif)富集统计;DAR阈值为校正后P<0.05,富集基序按FDR<0.05且log2enrichment ratio>1筛选。e,YA样本神经发生细胞的细胞特异性调控子(regulon)热图点图;若基于基因的AUC变化显著(BH校正、Mann–Whitney U检验、双侧、FDR<0.05),则纳入每类细胞最特异的前10个调控子。
3 由DAR驱动的改变
在建立YA队列的神经发生框架后,作者进一步比较不同年龄与认知诊断组对神经发生的影响。除YA外,研究还纳入健康老年(HA,8名供体,73,093个细胞核)、临床前中间病理(PCI,6名供体,58,281个细胞核)、阿尔茨海默病(AD,10名供体,87,209个细胞核)与超级老年人(SA,6名供体,51,437个细胞核)。在细胞类型层面,YA中观察到的细胞类型在其他队列中均可检测到。与HA相比,PCI与AD中NSC数量显著增加;而与HA与YA相比,AD中神经母细胞与未成熟神经元的平均数量显著减少,且AD中的未成熟神经元数量也显著低于PCI。
更关键的是,神经发生在“年龄驱动”与“诊断驱动”条件下的改变,主要体现在DAR数量的变化而非DEG数量的变化,这提示以染色质可及性为代表的表观遗传差异,可能比mRNA差异更能稳定刻画衰老相关的认知差异。作者指出,大多数DEG出现在NSC中;以文中统计为例,AD与HA之间仅有172个DEG,AD与PCI之间仅有6个DEG,AD与YA之间为154个DEG,而SA与其他诊断队列之间为18个DEG。与此同时,NSC中上调与下调的DEG与DAR数量在年龄与诊断比较中大致相当。将所有神经发生细胞合并后,AD组在基因与开放染色质区域的变化方向上与其他条件呈现相反趋势。进一步的DAR基序富集分析显示,差异可及区域中最显著的基序多属于锌指转录因子家族,而下调最明显的基序多属于RFX家族;二者均与发育、细胞生长与分化相关,提示调控轴可能在认知衰退过程中发生系统性切换。
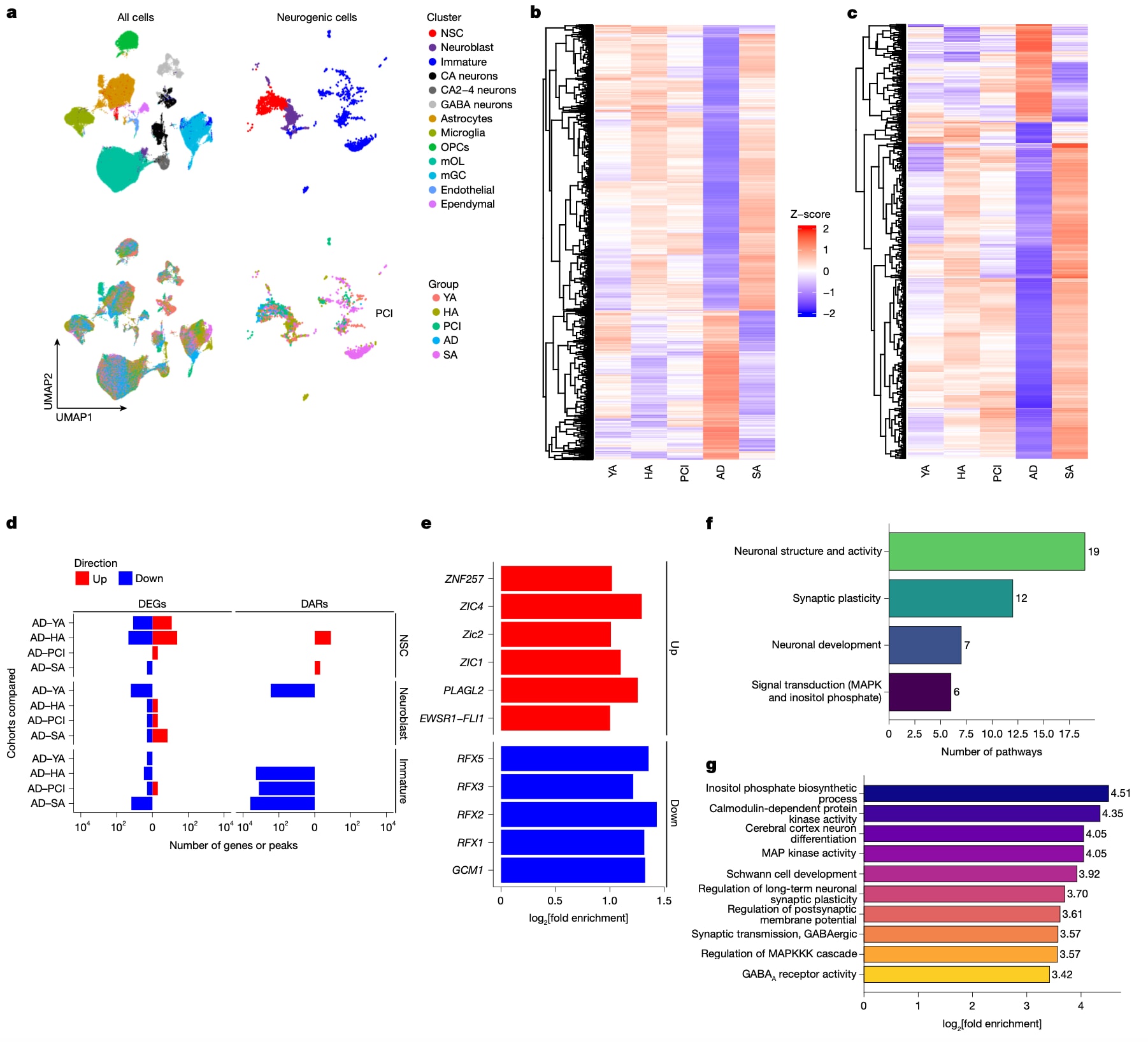
图2|随年龄与认知诊断变化的差异表达与开放染色质。 a,所有细胞(左)与神经发生细胞(右)的UMAP,可按细胞类型(上)或诊断组(下)着色。b,c,神经发生相关DEG(b)与DAR(c)的热图。d,不同诊断条件下神经发生相关DEG与DAR数量。e,不同诊断条件下神经发生相关的关键基序变化。f,g,对PCI中上调、且可能指向向AD过渡的关键DAR推断靶基因做通路富集分析:f按通路丰度(P<0.05;log2FC)展示,g按log2 fold enrichment展示。
作者进一步识别到一组在PCI队列中特异下调的DAR,这些DAR主要出现在神经母细胞与未成熟神经元中,相较YA、HA与SA均降低,并在AD中进一步下调。基于这一观察,作者提出:PCI阶段的开放染色质异常可能早于相应的RNA表达变化。为把这些差异与调控网络连接起来,作者将上述峰集合并到GRN分析中推断靶基因,并进一步开展通路富集。结果显示,被牵引的通路多与神经元结构与功能维持、突触可塑性与神经元发育相关。综合来看,这些结果提示:随认知恶化发生的神经发生异常可能由DAR的下调所驱动,而年龄相关最早的改变更可能出现在NSC;同时,AD组神经母细胞与未成熟神经元中的多数DAR与DEG呈现明显下调,其中与突触可塑性与神经递质传递相关的DAR,可能构成神经发生病理性改变的早期信号。
4 年龄与诊断相关的调控网络
在识别到神经发生的差异主要由染色质可及性驱动后,作者进一步希望厘清哪些基因调控网络(GRN)在衰老与疾病中主导这些变化。为此,研究使用SCENIC+将单细胞染色质可及性与基因表达信息结合,并通过基序发现推断增强子驱动的GRN(eGRN),从而得到增强子驱动的调控子集合(eRegulon)。在eRegulon嵌入空间中,NSC构成一个清晰独立的簇,提示其在调控网络层面也具有鲜明特征。基于eRegulon的扩散分析进一步支持NSC、神经母细胞与未成熟神经元之间存在谱系连续性。
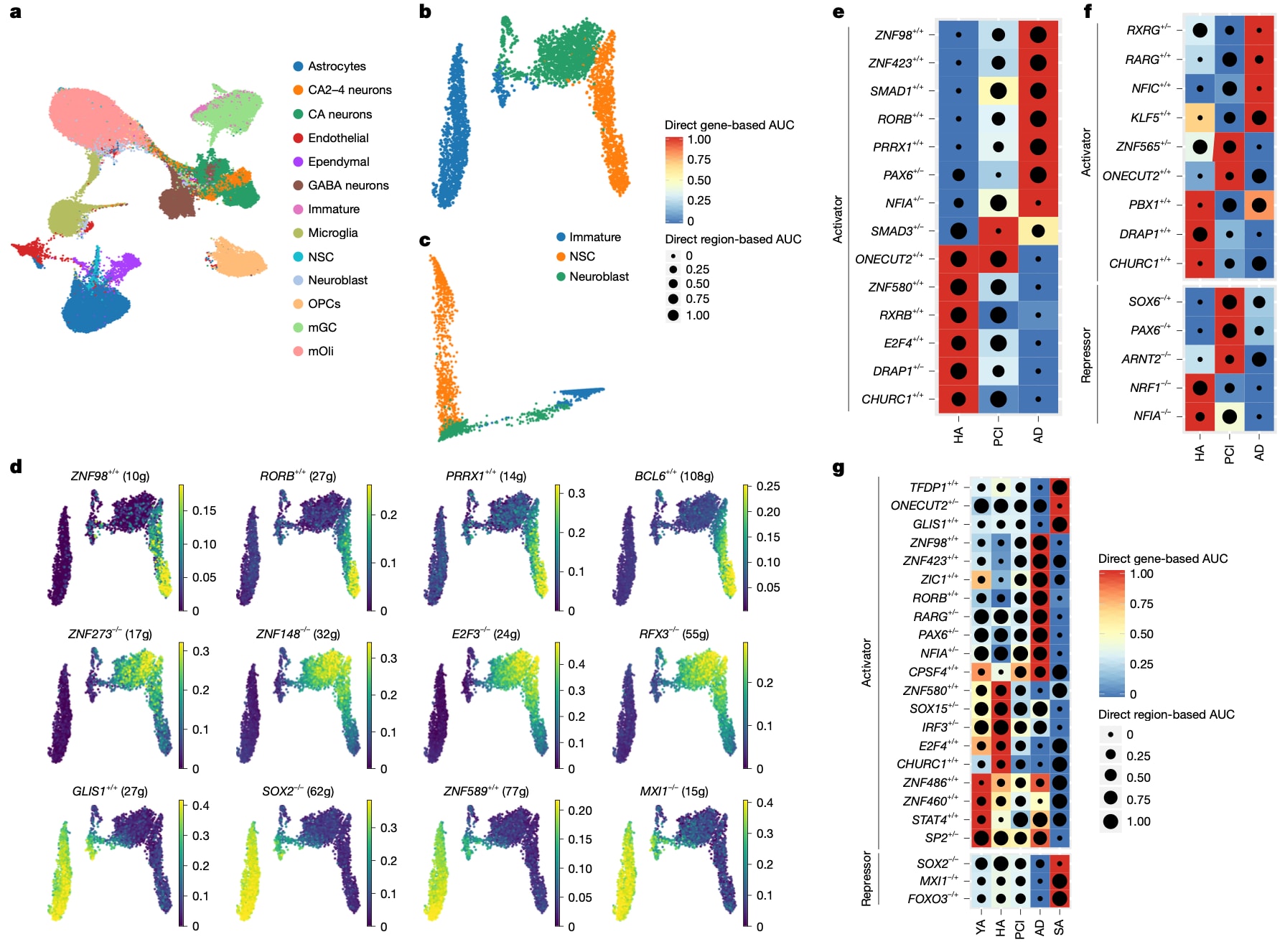
图3|衰老与认知衰退中的GRN。 a,基于SCENIC+eRegulon嵌入,对所有条件下的全部细胞进行UMAP可视化。b,c,基于SCENIC+eRegulon嵌入,对神经发生细胞进行UMAP(b)与扩散图(c)可视化。d,将每类神经发生细胞最特异的前4个调控子的“基于基因的AUC活性分数”投影到UMAP;行顺序依次为NSC、神经母细胞、未成熟神经元;颜色表示调控子活性,仅展示显著的细胞特异eRegulon(BH校正、Mann–Whitney U检验、双侧、FDR<0.05);括号内为每个调控子包含的靶基因数量(对应g)。e,HA、PCI、AD三组中所有神经发生细胞的差异调控子。f,HA、PCI、AD三组中NSC的差异eRegulon。g,所有认知诊断条件下神经发生相关的差异eRegulon。对e~g而言,若基于基因的AUC变化显著(BH校正、Mann–Whitney U检验、双侧、FDR<0.05),则按fold change为每个条件纳入前5个调控子。
在认知衰退相关的调控网络层面,作者比较PCI与AD相对HA的变化,发现HA条件下驱动神经发生的一组关键eRegulon在PCI与AD中被下调,其中前6个关键eRegulon里有5个在PCI与AD中下降;与之相对,另一组eRegulon在PCI中上调,并在AD中进一步上调。值得注意的是,在这7个上调的eRegulon中,有5个(ZNF98、SMAD1、RORB、PRRX1、NFIA)正是YA队列NSC的主导eRegulon之一,这可能部分解释了AD中NSC数量的显著上升。进一步的细胞类型特异分析提示,这种变化可能与PCI与AD中NSC的NFIA抑制子下调有关。
作者还观察到,在HA、PCI与AD三类认知队列中,NSC由不同组合的激活子与抑制子eRegulon共同调控:在PCI中,上调的激活子包括ZNF565与ONECUT2,而抑制子包括SOX6、PAX6与ARNT2;在AD中,这些因素被另一组激活子所替代,包括RXRG、RARG、NFIC与KLF5。将视角扩展到所有诊断条件后,作者总结出三点:其一,SA相对其他条件呈现独特特征,激活子TFDP1、ONECUT2、GLIS1以及抑制子SOX2、MXI1、FOXO3上调;其二,AD中存在一组“特异上调”的激活子特征,而其他多数组合显著下调,其中包含ZNF98、ZNF423、ZIC1、RORB、RARG、PAX6、NFIA与CPSF4;其三,还存在一组明显由衰老驱动的特征,代表性激活子包括ZNF580、SOX15、IRF3、E2F4与CHURC1。整体而言,这些结果支持:随认知诊断变化的神经发生异常,受到不同cis调控元件、转录因子与靶基因之间网络互作重排的驱动。
5 神经发生的韧性特征
在明确认知衰退伴随神经发生异常后,作者把焦点转向“认知韧性”,尤其是超级老年人(SA)队列。细胞丰度分析显示,SA中未成熟神经元数量相较其他队列显著增加。作者注意到该差异可能受到单个未成熟神经元数目极高的样本影响,但即便剔除该离群样本,未成熟神经元数量仍可观察到2.5倍增加;并且SA相对AD的未成熟神经元丰度差异在是否剔除离群样本的设定下均保持显著。SA相对HA、YA与PCI也呈现约2倍增加,但统计上未达显著。除未成熟神经元外,SA中的神经母细胞数量也显著高于AD(q=0.0002)。
从分子层面看,SA队列神经发生特征的差异主要由DAR驱动:与其他队列相比,SA中未成熟神经元有7,058个DAR上调,神经母细胞有674个DAR上调,而NSC中仅观察到较少改变。与大量DAR变化相对,转录层面的差异基因较少,但仍包含一些关键分子,例如神经母细胞与未成熟神经元中上调的BDNF(brain-derived neurotrophic factor)与CALB1,以及下调的NEUROD6与NECTIN3(后者与载脂蛋白E(APOE)相关并被认为参与突触可塑性)。
为检验是否存在可重复的“韧性特征”,作者构建了韧性分数(resilience score),用于捕捉AD相对YA、HA与SA的改变是否呈现一致方向。具体而言,作者对每个比较计算fold change,并以这些fold change乘积的几何平均定义韧性分数。结果显示,韧性特征在神经母细胞与未成熟神经元中最为清晰:多数基因与开放染色质峰在YA、HA与SA中相对稳定,却在AD中显著下调;这一模式在开放染色质区域上更为夸张。相较之下,NSC中的部分基因与峰会随年龄或诊断状态发生变化,提示其更可能承载“早期改变”或“状态切换”的信号。
对每种细胞类型排名前500的韧性基因进行通路富集(FDR<0.05)显示:NSC更偏向增殖与生长等细胞过程;神经母细胞更偏向线粒体与内体相关通路以及突触小泡内吞;未成熟神经元则富集RNA结合、蛋白结合、细胞质与轴突相关通路。对未成熟细胞中排名前500的韧性开放染色质峰进行基序富集(FDR<0.05)进一步提示,其富集的转录因子基序多与促进神经元分化的锌指蛋白相关;同时需要注意,NSC或神经母细胞的韧性峰并未观察到显著的基序富集。
为解析韧性背后的调控网络,作者进一步比较SA的eRegulon谱。总体上,YA与SA在NSC与未成熟神经元中共享一部分共同eRegulon:例如,SA的NSC中主要激活子包括ZNF98、SOX6、RORB、PRRX1、ETV6与BCL6,共同抑制子包括SOX2与MXI1;而YA与SA的未成熟神经元共享的激活子eRegulon包括ZNF589、TFDP1、ONECUT2、MTF2、MTA3、GLIS1与E2F3,共同抑制子同样包含SOX2与MXI1。与此同时,SA也呈现独特eRegulon,例如未成熟神经元的PROX1激活子eRegulon,以及NSC中的ZNF423、ZIC1、SOX2与NFE2L2等;并且SA的NSC出现一系列在YA中不活跃的抑制子。
值得注意的是,YA队列的神经母细胞表现出与分化相关的强eRegulon程序,由NEUROD1、FEZF2、EGR1、EGR3、E2F1与THRA等驱动;这一协同程序在SA中基本缺失,SA神经母细胞中仅保留SOX2与NFE2L2等少数激活子,而更多表现为一组在YA中不活跃的抑制子。这些差异提示,YA与SA在神经发生的转录调控景观上存在系统性偏移。进一步的跨队列比较也显示,SA相对其他诊断队列存在独特的eRegulon变化:在未成熟神经元与神经母细胞中,特定eRegulon集合显著上调,而多数激活子与抑制子整体下调;在神经母细胞中,还可见NEUROD1与NRF1抑制子下调,同时FOXO3与MXI1抑制子上调。NSC中多数激活子与顶部抑制子下调,可能部分解释SA的NSC中DEG与DAR相对稀少。
作者进一步追问SA的独特特征是否仅由衰老驱动。分析提示,SA确实包含部分“衰老效应”,但多数变化独立于衰老:例如,在NSC中,激活子E2F1与抑制子NFIB在HA与SA中均下调,可能代表衰老诱导的改变;同样,YA中占主导的激活子CEBPZ在HA与SA中下调。然而,相较HA,SA的NSC与未成熟神经元仍表现出一组更具特异性的上调激活子,例如NSC中的ZBTB21、NFE2L2、MBNL2、FOS、EGR4与EGR1,以及未成熟神经元中的ZBTB7A、NFE2L1、ELK1与EGR3。作者也指出,仍不能完全排除这些独特eRegulon来自衰老驱动的可能性,因为神经母细胞在HA与SA之间的谱系轮廓更为相近。总体而言,这些结果指向SA中存在一套特异的神经发生分子网络,可能与其更优的认知表现相关。
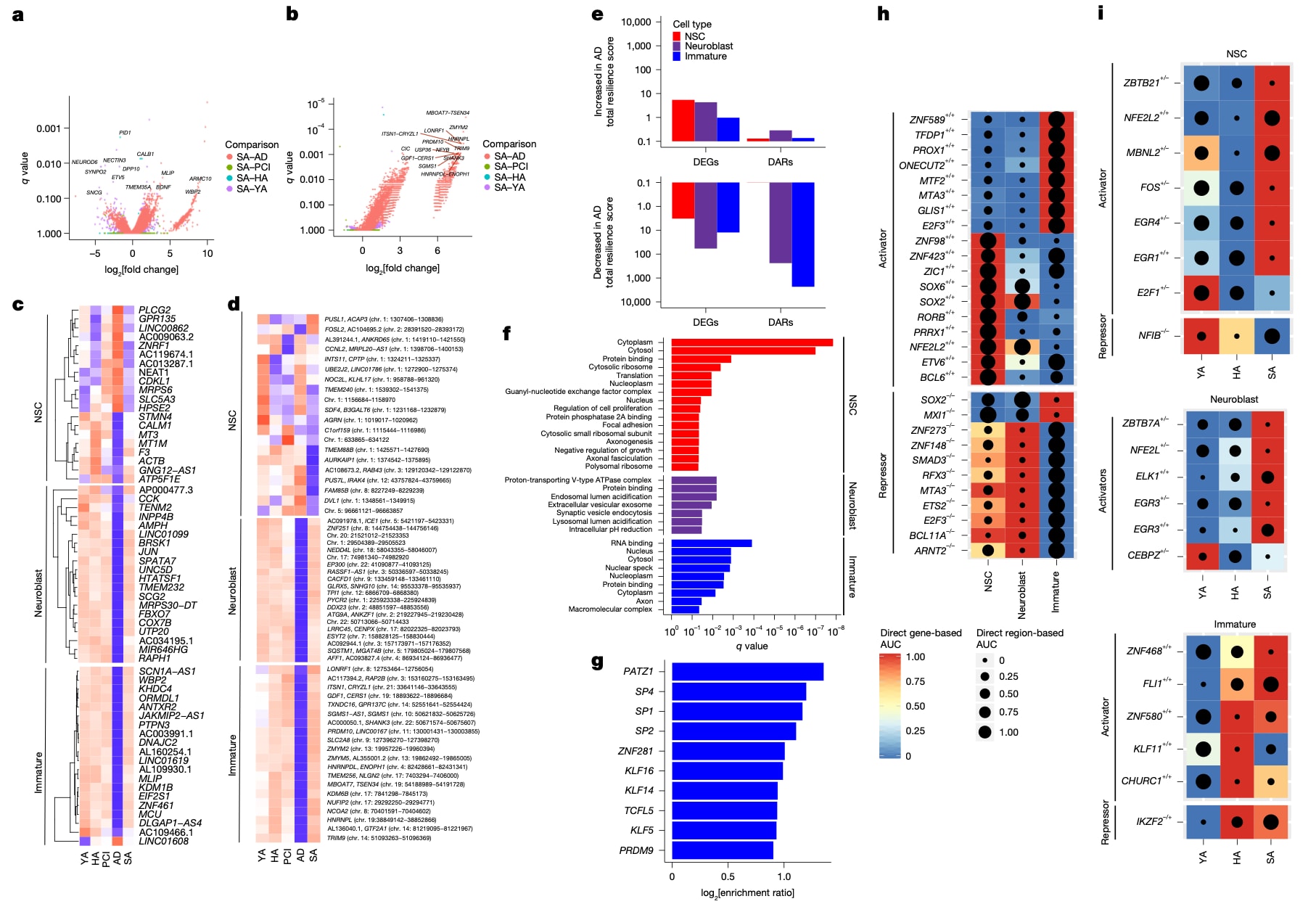
图4|神经发生的韧性特征。 a,b,SA队列未成熟神经元相对其他认知诊断条件的前列DEG(a)与DAR(b)。c,d,各细胞类型的前20个韧性基因(c)与开放染色质峰(d)。e,各细胞类型的总韧性分数,对全部基因或开放染色质峰求和,并按其在AD中的相对效应分为增加(上)或减少(下)。f,每种细胞类型前500个韧性基因的富集通路(FDR<0.05)。g,未成熟细胞前500个韧性开放染色质峰的富集基序(FDR<0.05);注意NSC或神经母细胞的韧性峰未见富集基序。h,SA组神经发生细胞的细胞特异调控子;若基于基因的AUC变化显著(BH校正、Mann–Whitney U检验、双侧、FDR<0.05),则纳入每类细胞最特异的前10个调控子。i,NSC、神经母细胞与未成熟神经元在SA对HA以及SA对YA比较中的差异调控子;若基于基因的AUC变化显著(BH校正、Mann–Whitney U检验、双侧、FDR<0.05),则按fold change为每个条件纳入前5个调控子。
6 成功或失败的衰老
在韧性神经发生之外,作者进一步尝试定位决定“成功衰老”与“病理衰老”的海马网络信号。研究提出海马认知完整性(HIPPI)这一分析视角:筛选在SA相对HA差异表达、且在PCI相对HA与YA呈现相反趋势的分子信号,以刻画从健康衰老走向病理衰老的分叉点。该分析共得到1,001个DEG与579个DAR,其中DEG主要集中在CA1神经元,而DAR主要集中在星形胶质细胞;此外,少突胶质祖细胞(OPC)与成熟少突胶质细胞(mOL)中也可见显著改变。
在CA1神经元中,最显著的HIPPI相关基因多与神经元功能与神经递质传递有关,例如GABRB1、NRGN与KCNF。与此同时,微胶质细胞中的APOE,以及EGR1与GRASP等分子也值得关注,它们可把受体(包括第一组代谢型谷氨酸受体)与神经元蛋白连接起来。作者还指出其他细胞类型中的关联信号,例如抑制性神经元中的GRM8,以及成熟颗粒细胞(mGC)中的KCNE、GRIN2B、GRIA1与GRIK1等。综合而言,维持高效的神经递质传递、突触可塑性与氧化还原平衡,可能是成功认知衰老的核心特征;相反,这些过程的破坏可能标记向PCI的过渡。
除突触与细胞稳态外,CA神经元的HIPPI基因通路富集还覆盖细胞质核糖体、能量代谢,以及线粒体、内体与溶酶体相关过程。星形胶质细胞的DAR及其基序分析则揭示大量FOS–JUN碱性亮氨酸拉链因子(bZIP)。为评估HIPPI相关DEG与DAR对神经发生的影响,作者进一步在神经发生细胞、星形胶质细胞与CA1神经元之间开展CellChat配体–受体信号分析;并在星形胶质细胞与CA1神经元中对各诊断组的GRN进行比较,计算跨诊断组的“衰老分数”,以衡量相同TF–peak–gene互作强度的变化。
结果显示,最显著的互作通路集中在突触黏附与兴奋性传递相关复合体,例如neurexin–neuroligin(NRXN1–NLGN)轴,并包含与AD相关的calsyntenin样蛋白(如NRXN1–CLSTN1与NRXN1–CLSTN2)、NCAM1、contactin(CNTN)、APP–SORL1以及多类谷氨酸能受体组合(例如Glu-SLC17与GRIA家族、Glu-SLC17与GRIK2、Glu-SLC17与GRM家族)。SA与HA中增强的突触黏附与谷氨酸能通信,与PCI与AD中该信号的减弱形成对照。这提示保持兴奋性突触完整性可能是健康认知衰老的标志,也可能成为预防认知恶化的潜在干预靶点。
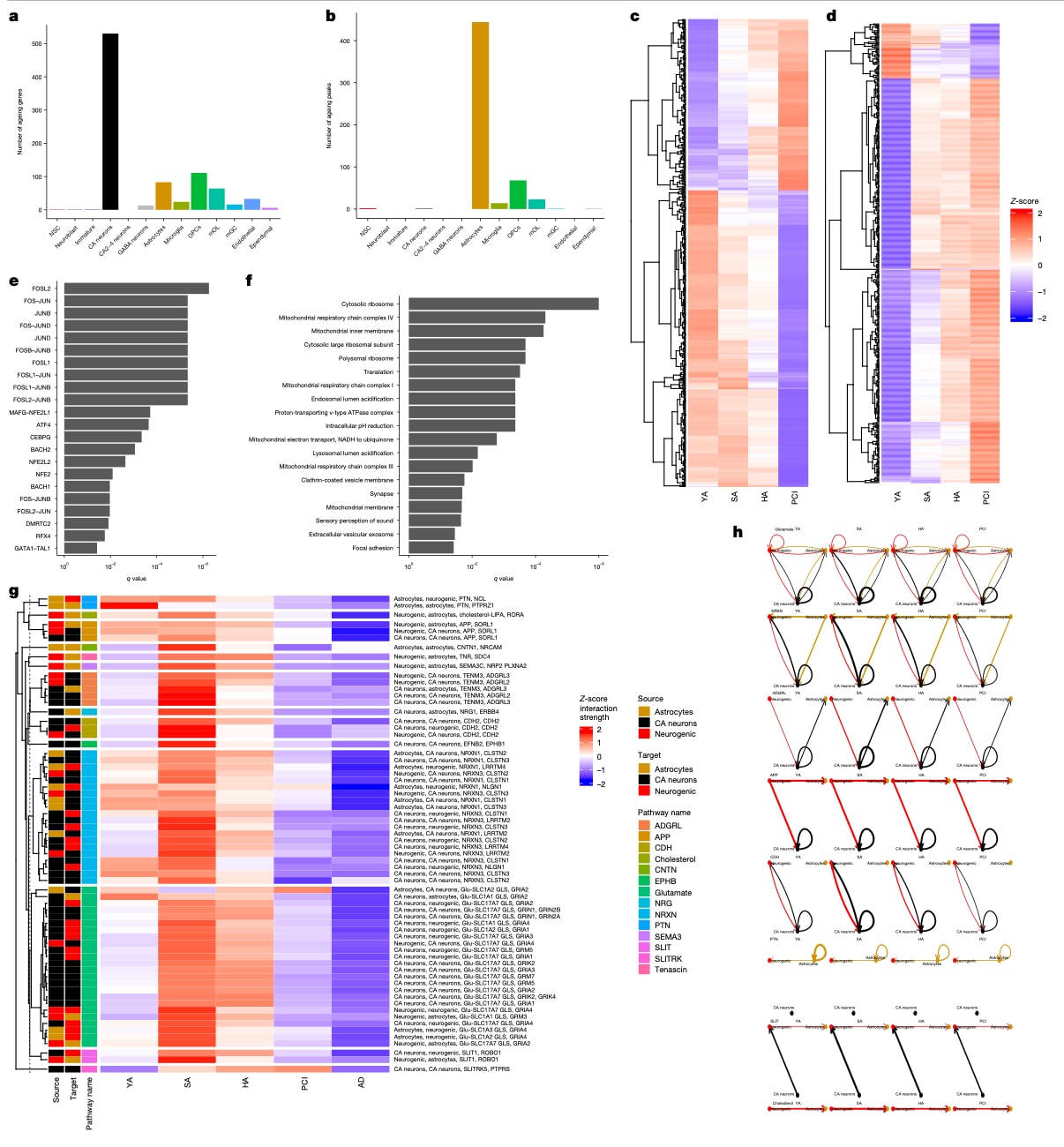
图5|成功与失败衰老中的海马网络。 a,b,在海马各细胞类型中,HA与SA相对PCI呈相反表达模式的DEG数量(a)与DAR数量(b)。c,d,CA神经元DEG(c)与星形胶质细胞DAR(d)的热图。e,CA神经元中在健康衰老与病理衰老(PCI)之间呈相反调控的显著通路(q<0.05)。f,星形胶质细胞DAR中在健康与病理衰老之间呈相反可及性变化的显著富集基序(q<0.05且log2 ratio>1)。g,h,基于衰老筛选后的CellChat变化,展示相互作用相对强度的热图(g)与网络图(h)。
7 讨论
该研究通过对不同认知功能状态人群的海马样本进行snRNA-seq与ATAC-seq整合分析,给出若干对“成人神经发生”“认知衰退”“认知韧性”与“衰老网络”的关键洞见。
第一,作者在20~40岁、无已知认知缺陷且无痴呆相关蛋白病理的年轻成人样本中,系统刻画了成人海马的神经发生分子网络,观察到从NSC经由神经母细胞与未成熟神经元走向成熟颗粒神经元的轨迹。NSC簇内部还包含潜在时间不同的多个亚状态,可能对应不同状态的NSC与神经祖细胞。作者指出,更高灵敏度的分析有望进一步提高NSC亚群的分辨率。研究还将该神经发生特征与既往齿状回神经发生研究进行对照,并应用于多个大规模全脑scRNA-seq数据集:多数脑区未见NSC,与“成人神经发生主要局限于海马齿状回”等观点一致;少量在其他脑区偶见的NSC样细胞,可能源于冷冻组织块的粗略取材导致齿状回细胞混入。为降低这一风险,作者强调该研究对每块冷冻组织均验证了齿状回的存在,并进行了激光显微切割以富集齿状回区域;综合个体差异与队列差异后,作者认为该研究的NSC注释具有可靠性。
第二,研究显示神经发生不仅体现为一组共享基因,还呈现出与细胞成熟阶段相匹配的开放染色质与调控网络特征,从而在“转录—表观遗传—调控网络”三层面共同界定细胞表型与成熟度。
第三,作者比较不同年龄与诊断组后认为:随衰老与认知诊断变化的最早改变更可能发生在NSC,并在AD中演化为神经母细胞与未成熟神经元层面更显著的DAR重塑。研究还识别出PCI中特异的DAR集合,可能代表由临床前阶段走向AD的分子进展轨迹;这些DAR关联的下调通路与突触可塑性与神经递质传递有关,提示对相关通路的干预可能有助于减缓或阻止AD中神经发生的进一步恶化。
第四,在调控网络层面,作者识别出与年龄与认知衰退相关的一组eRegulon组合,并提出对这些网络的靶向可能帮助预防或缓解神经发生异常,从而在机制上影响认知衰退过程。
第五,研究提出神经发生存在“韧性特征”:除SA相对其他队列的差异基因、开放染色质区域、通路与基序外,作者还重点关注在YA与HA中出现、在SA中被维持、而在PCI与AD中呈相反方向的信号组合,认为其可能对应维持衰老期认知完整性的调控机制。作者也强调,SA中未成熟神经元数量总体增加,但细胞丰度在样本间变异很大且样本量有限,限制了该部分的定量统计能力;未来需要更大规模的人脑样本开展验证。
在局限方面,作者指出多组学人脑研究天然受到样本量与个体差异的限制。随着多组学测序更广泛地应用于具有明确认知表型的人脑样本,后续研究将更好地评估“染色质可及性差异”与“mRNA表达差异”之间的稳定性差别。文中也提出两种可能解释:其一,DEG数量少而DAR数量多,可能反映mRNA稳定性对样本采集与处理方式更敏感,而DNA层面的可及性相对不受采集时间与流程差异影响;其二,mRNA差异可能更多代表脑对刺激的急性响应,而染色质可及性更可能是更稳健的“底层状态”指标。
第六,作者认为SA中的神经发生由一套不同的GRN组合主导,提示“韧性”不仅是量的差异,也可能是调控架构的差异。
最后,研究在海马网络层面识别出与健康认知衰老相关的HIPPI信号:相关改变主要体现为CA1神经元的DEG与星形胶质细胞的DAR,并可由谷氨酸能通路牵引的细胞—细胞互作把CA1、星形胶质细胞与神经发生连接起来。作者据此提出,这些互作可能决定成功与失败衰老的分叉,并进一步影响AD中CA1神经元的减少。总体而言,该研究描绘了海马神经发生的多组学分子特征及其随年龄与认知状态变化的轨迹,并强调跨神经发生谱系的表观遗传差异可能比单纯基因表达更能界定不同衰老相关认知受损路径;相关发现也突出了进一步解析机制、从而发展面向衰老期认知保护的靶向治疗策略的重要性。